利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。T℃时反应2SO2(g)+O2(g) 2SO3(g)过程中的能量变化如图所示,回答下列问题。
2SO3(g)过程中的能量变化如图所示,回答下列问题。
(1)T℃时将3mol SO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol , 则达到平衡时SO2的转化率为 。(1分)
SO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol , 则达到平衡时SO2的转化率为 。(1分)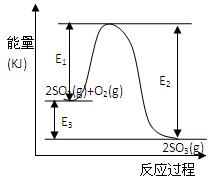
(2)下列叙述能证明该反应已达化学平衡状态的是 (填序号)(2分)
①SO2的体积分数不再发生变化 ②容器内压强不再发生变化 ③容器内气体分子总数不再发生变化 ④相同时间内消耗2n molSO2的同时生成n molO2 ⑤相同时间内消耗2n molSO2的同时生成2n mol SO3
SO3
(3)反应 (填“放出”或“吸收”) 热量(用E1、E2或E3表示)(2分)。
(4)若以下图所示装置,用电化学原理生产硫酸,将SO2、O2以一定压强喷到活性电极上反应。
写出两电极的电极反应式: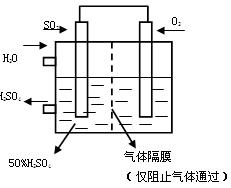
; 。(2分) [来网]为稳定持续生产,硫酸溶液的浓度应维持不变,则通入S O2和水的质量比为 (2分)
O2和水的质量比为 (2分)
现有下列10种物质:①水;②空气;③二氧化碳;④醋 酸;⑤熟石灰;⑥胆矾(CuSO4·5H2O);⑦氢氧化铁胶体;⑧硫酸钠;⑨硫酸铵;⑩铁。
酸;⑤熟石灰;⑥胆矾(CuSO4·5H2O);⑦氢氧化铁胶体;⑧硫酸钠;⑨硫酸铵;⑩铁。
请将以上物质的序号填在所属类别的横线上:属于混合物的是;属于氧化物的是;属于单质的是;
从电离的角度分类,属于酸的是,属于碱的是;属 于盐的是;属于非电解质的是。
于盐的是;属于非电解质的是。
在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:
请回答:
① A电极对应的金属是______(写元素名称),B电极的电极反应式是。
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
。
如图所示,常温下电解5 min后,铜电极质量增加2.16g。试回答: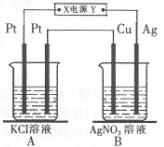
(1)电源电极X名称为(填“正极”或“负极”)。
(2)电解池B中阳极的电极反应式是。
(3)若A中KCl溶液的体积是200mL,电解后溶液的PH=(忽略电解前后溶液体积的变化)。
若要使电解后的溶液恢复到与电解前完全相同,应加入。
如下图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。
(1)打开K2,合并K1。B为极,A的电极反应为,最终可观察到的现象是
涉及的化学反应方程式有:
(2)打开K1,合并K2。E为极,F极的电极反应为,检验F极产生气体的方法是。
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是,原因是
按要求填空:
(1)拆开1 mol H—H键,1 mol N—H键,1 mol N≡N键分别需要吸收的能量为436 kJ,391 kJ,946 kJ。则理论上1 mol N2生成NH3___________热量(填:“吸收”或“放出”) _______kJ;事实上,反应的热量总小于理论值,理由是_______________________。
(2)X、Y两元素能形成XY2型化合物,XY2中共有38个电子,若XY2是离子化合物,其化学式是___________;若XY2是共价化合物其结构式是____________。
(3)第三周期内,X、Y两元素的原子序数之差为4,它们组成的XY型化合物,其电子式为____________。
(4)某非金属X的最高正价为+m,它的最高价氧化物对应的水化物中有b个氧原子,则这种酸的化学式是____________。
(5)X元素的最高正价和负价绝对值之差为6,Y元素和X元素原子的次外电子层上都有8个电子,X和Y形成的化合物YX2在水溶液中能电离出电子层结构相同的离子,用电子式表示该化合物的形成过程______________