下列关于热化学反应的描述中正确的是
| A.已知H+(aq)+OH-(aq)== H2O(l)ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3) kJ·mol-1 |
| B.葡萄糖的燃烧热是2800 kJ·mol-1,则1/2C6H12O6(s)+3O2(g)==3CO2(g)+3H2O(l)ΔH=1400 kJ/mol |
| C.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)==2H2(g)+O2(g)ΔH=+571.6 kJ·mol-1 |
| D.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+1/2O2(g)== CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,CH3OH(g)的燃烧热为192.9 kJ·mol-1 |
已知A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族,下列推断不正确的是()
A. D一定在第二周期 B. A、B、D不可能在同周期
C.A、D可能在同一主族 D.C和D的单质可能化合为离子化合物
下列关于价电子构型3s23p4的描述正确的是( )
| A.它的元素符号为O |
| B.它的核外电子排布式为1s22s22p63s23p4 |
| C.可以与H2化合生成液态化合物 |
D.其轨道表示式为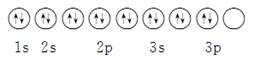 |
下列有关化学键与物质结构的说法正确的是()
| A.两种元素组成的分子中一定只有极性键 |
| B.分子中的价电子对(包括成键电子对和孤电子对)之间存在相互排斥作用 |
| C.非金属元素组成的化合物一定是共价化合物 |
| D.含有阳离子的物质一定含有阴离子 |
科学家最近发现两种粒子:第一种是由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第二种是由四个氧原子构成的分子。下列有关这两种粒子的说法不正确的是()
| A.“四中子”的粒子不显电性 | B.“四中子”的质量数为4 |
| C.第二种粒子是氧元素的另一种同位素 | D.第二种粒子的化学式为O4 |
下列各项叙述中,正确的是()
| A.用电子云图形象地描述电子在空间单位体积内出现概率的大小 |
| B.在同一电子层上运动的电子,其自旋方向肯定不同 |
| C.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| D.原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解 |