已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
| A.AgCl>AgI>Ag2CrO4 | B.AgCl>Ag2CrO4>AgI |
| C.Ag2CrO4>AgCl>AgI | D.Ag2CrO4>AgI>AgCl |
下列检验离子的方法及结论正确的是()。
| A.向某溶液中滴加AgNO3溶液后产生白色沉淀,说明原溶液中含有Cl- |
| B.向某溶液中滴加BaCl2溶液后产生白色沉淀,说明原溶液中含有SO42- |
| C.向某溶液中滴加NaOH溶液后生成蓝色沉淀,说明原溶液中含有Cu2+ |
| D.向某溶液中滴加稀硫酸后生成无色无味的气体,说明原溶液中含有CO32- |
下列溶液中不存在氯离子的是:………………………()
| A.氯水 | B.氯化钠溶液 | C.漂白粉溶液 | D. 氯酸钾溶液 氯酸钾溶液 |
下列除去杂质的方法正确的是()
| A.除去CO2中的少量HCl:通入NaOH溶液 |
| B.除去NaOH溶液中的少量MgCl2:加入适量KOH溶液,过滤 |
| C.除去KCl溶液中的少量K2CO3:加入适量的盐酸 |
| D.除去N2中的少量O2:通过灼热的CuO粉末 |
下列各组离子在溶液中能大量共存的是……………………()
A.Ba2+、C1-、 、K+ 、K+ |
B.Fe3+、OH-、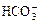 、Na+ 、Na+ |
C.Ca2+、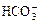 、C1-、K+ 、C1-、K+ |
D.Ag+、 、Cl-、K+ 、Cl-、K+ |
质量相等的下列物质中,含分子数最多的是()
| A.CH4 | B.O2 |
C.NH3 |
D.CO |