钙、镁、铝等的化合物在生产生活中有着广泛的应用。甲、乙两研究小组分别对石灰乳吸收硝酸工业的尾气、碱式碳酸镁铝[MgaAlb(OH)c(CO3)d·xH2O]的有关问题进行了以下探究,请你参与并完成对有关问题的解答。
(1)甲组利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得有广泛应用的Ca(NO2)2,其部分实验流程如下: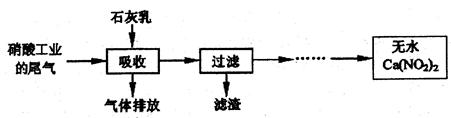
①大量氮氧化物排放到空气中,会破坏臭氧层,形成酸雨等,由氮氧化物形成的酸雨称为是_________(填“硫酸”或“硝酸”)型酸雨。过滤操作中,需要使用的玻璃仪器有烧杯、玻璃棒和_______________。
②上述流程中采用“气一液逆流接触”吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是_________________;滤渣可循环使用,滤渣的主要成分是________。
(2)乙组查阅有关资料知道碱式碳酸镁铝受热容易分解,因此在生产生活中常用作塑料阻燃剂。
①MgaAlb(OH)c(CO3)d·xH2O中a、b、c、d的代数关系式为______________________。
②根据你的理解,你认为碱式碳酸铝镁具有阻燃作用的可能原因主要是由于其受热分解需吸收大量热量和_______________________________。
③为确定碱式碳酸铝镁的组成,进行如下实验:准确称取6.780 g样品与足量稀盐酸充分反应,生成CO2 1.120 L(已换算成标准状况下)。另取一定量样品在空气中加热,样品的固体残留率随温度的变化如图所示(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物)。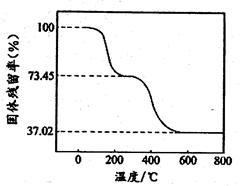
注意:固体残留率是指 。则在270℃~600℃之间,物质受热分解放出的气体是__________(填化学式)。6.780 g样品中,除结晶水外还含有的氢原子的物质的量是__________mol。
。则在270℃~600℃之间,物质受热分解放出的气体是__________(填化学式)。6.780 g样品中,除结晶水外还含有的氢原子的物质的量是__________mol。
常温下某淡黄色固体单质A,与它的气态氢化物B和氧化物C之间,有如右图的转变关系,试回答:
(1)A是、B是、C是。
(2)B的物质的量为x,氧气的物质的量为y,则当B跟氧气恰好反应,完全转化为A时,x与y的数值关系为;若当B转化为C时,反应后,常温下体系中只有C一种气体, x与y的数值关系是。
有一可左右滑动的密封导热隔板,当拔起销钉后,两侧分别开始进行如图所示的可逆反应,隔板随之开始移动。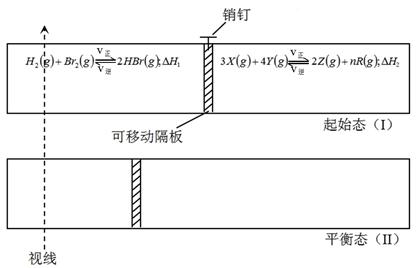
各物质的起始加入量
| 物质 |
H2 |
Br2(g) |
HBr |
X |
Y |
Z |
R |
| 物质的量(mol) |
2.0 |
2.0 |
5.0 |
设x |
8.0 |
0.50 |
1.5 |
当x在一定范围内变化时,均可因为隔板的导热作用而调节反应器左右两侧的温度,使两侧反应都达到平衡。在整个反应过程中隔板始终左滑,一段时间后,隔板恰好处于反应器左端1/3处不动,达平衡后保持温度不变。试回答:
(1)化学方程式中R物质的化学计量数n为(填编号,下同)
A.3 B.4 C.5 D.6
(2)若x=6.5,则右侧反应在起始时向方向(填“正反应”或“逆反应”)进行;欲使起始反应维持向该方向进行,则x的取值范围为。
(3)若已知ΔH 1<0,ΔH 2<0, x分别为6.5和7.0时,在这两种情况下,反应分别达到平衡状态(Ⅱ)时,请比较H2体积分数(分别记作φ(H2)、φ(H2’))的相对大小。
A.φ(H2)>φ(H2’) B.φ(H2)<φ(H2’)
C.φ(H2)=φ(H2’) D.不能确定
(4)若x=6.5时,左右两侧反应体系达平衡后,设法向左侧容器中再充入a mol氢气,当左、右两侧反应体系再次平衡时(隔板平衡点位置不变,下同)a的取值范围是。
(5)若x=6.5时,且左右两侧反应体系均达到平衡后,如向右侧反应体系中充入b mol氦气,片刻后,使容器两侧又均达到平衡。则右侧化学平衡将向方向(填“正反应”或“逆反应”)移动;b的最大值应小于。
A、B、C、D、E、F六种元素均是短周期元素,且原子序数依次增大。B、F原子的最外层电子数均为其电子层数的两倍,D、F元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙)转化关系如图(反应条件略去),元素E形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题:
(1)写出M与甲的浓溶液加热时反应的化学方程式。
(2)X、Y、Z、W属于同一类物质,这类化合物固态时的晶体类型为;X、Y、W都能与Z反应,则Z的结构式为。
(3)将X、W与D2按1∶1∶n的物质的量之比通入Z中,充分反应后无气体剩余或生成,则n=,写出反应的化学方程式。
(4)化合物ED2与元素B形成的某种单质晶体类型相同,且在高温下能发生置换反应。若反应中B的单质被破坏1 mol共价键,则参加反应的化合物ED2的质量为g。
(5)元素B的另一种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,则12 g该晶体中含有NA个正六边形。
TiO2在工业生产和日常生活中有重要用途。
I.工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:
其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O。
(1)净化钛矿石时,是否需要除去杂质FeO?答:(填“需要”或“不需要”)。
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式。
答:。
II.TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Ti(同时产生O2):将处理过的TiO2作阴极,石墨为阳极,熔融CaCl2为电解液,用碳块作电解槽池。
(3)阴极反应的电极反应式为___________________________________。
(4)电解过程中需定期向电解槽池中加入碳块的原因是______________________。
“方法二”是先将TiO2与Cl2、C反应得到TiCl4,再用镁还原得到Ti。因下述反应难于发生:
TiO2 (s)+2Cl2 (g) TiCl4(l)+O2 (g)ΔH=+151 kJ·mol-1
TiCl4(l)+O2 (g)ΔH=+151 kJ·mol-1
所以不能直接由TiO2 和Cl2反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
(5)已知:C(s)+O2 (g) = CO2 (g)ΔH=-394 kJ·mol-1。请填空:
TiO2 (s)+C (s)+2Cl2 (g) = TiCl4 (l)+CO2 (g)ΔH= ______________
(6)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因。
答:____________________________________________。
(A)(12分)工业上以氯化钾和钛白厂的副产品硫酸亚铁为原料可得到硫酸钾、过二硫酸钠和铁红颜料等产品,该方法原料的综合利用率较高。
(1)基态钛原子的核外电子排布式为▲。
(2)TiCl4在常温下是一种无色液体,而FeCl3可用升华法提纯,则两种氯化物均属于▲晶体。
(3)SO42-和 S2O82-(过二硫酸根)结构中,硫原子均位于由氧原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。下列说法正确的是 ▲。
A.SO42-中存在σ键和π键且与PO43-离子互为等电子体
B.S2O82-中存在非极性键且有强氧化性
C.S2O82-比SO42-稳定且两者的氧元素的化合价相同
(4)KCl与MgO的晶体结构跟NaCl的晶体结构相似,则KCl与MgO两者中熔点高的是 ▲,原因是 ▲。
(5)硫与氯可形成化合物SCl2,则该分子中硫原子的杂化方式为 ▲,分子的空间构型为 ▲。
(6)在一定条件下铁形成的晶体的基本结构单元如下图1和图2所示,则图1和图2的结构中铁原子的配位数之比为 ▲。