(15分)利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体[A12(SO4)3•18H2O]。
I.实验室制取无色的无水AlBr3(熔点:97.5℃,沸点:263.3~265℃)可用如图所示装置,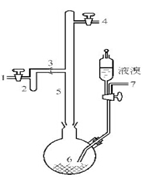
主要实验步骤如下:
步骤l.将铝箔剪碎,用CCl4浸泡片刻,干燥,然后投入到烧瓶6中。
步骤2.从导管口7导入氮气,同时打开导管口l和4放空,一段时间后关闭导管口7和1;导管口4接装有五氧化二磷的干燥管。
步骤3.从滴液漏斗滴入一定量的液溴于烧瓶6中,并保证烧瓶6中铝过剩。
步骤4.加热烧瓶6,回流一定时间。
步骤5.将氮气的流动方向改为从导管口4到导管口l。将装有五氧化二磷的干燥管与导管口1连接,将烧瓶6加热至270℃左右,使溴化铝蒸馏进入收集器2。
步骤6.蒸馏完毕时,在继续通入氮气的情况下,将收集器2从3处拆下,并立即封闭3处。
(1)步骤l中,铝箔用CCl4浸泡的目的是 。
(2)步骤2操作中,通氮气的目的是 。
(3)步骤3中,该实验要保证烧瓶中铝箔过剩,其目的是 。
(4)铝与液溴反应的化学方程式为 。
(5)步骤4依据何种现象判断可以停止回流操作 。
(6)步骤5需打开导管口l和4,并从4通入N2的目的是 。
II.某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH关系如图所示,实验中可选用的试剂:处理过的铝箔;2.0mol•L-1NaOH溶液:2.0 mol•L-1硫酸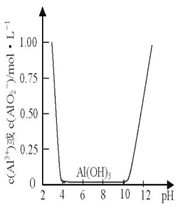
(7)由铝箔制备硫酸铝晶体的实验步骤依次为:
①称取一定质量的铝箔于烧杯中,分次加入2.0 mol•L-1NaOH溶液,加热至不再产生气泡为止。
②过滤 ③ ;
④过滤、洗涤 ⑤ ;⑥ ;
⑦冷却结晶; ⑧过滤、洗涤、干燥。
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯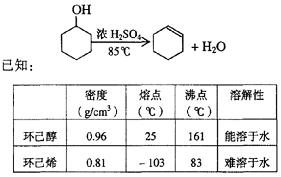

(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入l mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是____________。
②试管C置于冰水浴中的目的是______________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从_________口进入,目的是__________________。
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是()
a.蒸馏时从70 ℃开始收集产品 b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,
这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如下图所示的方案对废液进行处理,以回收金属,保护环
境。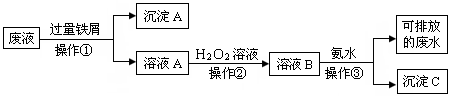
(1)操作①的名称是,沉淀A的成分是(填化学式)
(2)操作②反应时还需加入少量硫酸,操作②中观察到的实验现象是。
(3)操作②中发生反应的离子方程式为。
(4)检验可排放的废水中不含Fe3+的方法是:
(8分)某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。实验室可以用装置F制备氯气
请回答下列问题:
(1)装置F中发生反应的离子方程式为_____________________________;
(2)为了快速制备氨气,装置A的烧瓶中可装试剂____________________;
(3)E装置的作用是_______,DE的位置能不能调换(填“能”或“不能”);
(4)通入C装置的两根导管左边较长、右边较短,目的是_______________;
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式:__________________________________。
某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
| 实验步骤 |
实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 |
A. 浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色。 |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 |
B.有气体产生,溶液变成浅红色 |
| 3.将一小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,产生大量无色气体。 |
| 4.将镁条投入稀盐酸中 |
D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 |
E.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等。
仪器:①,试管,试管夹,烧杯,镊子,小刀,玻璃片,砂纸,酒精灯等。
(3)实验内容:(将与实验步骤对应的实验现象的编号和离子方程式填在答题卷上)
(4)实验结论:。
无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂,工业上作防腐剂、制造白色颜料(锌钡白)等。某实验小组欲用制氢废液制备硫酸锌晶体,进行了以下实验:
(1)取50mL制氢废液,过滤。除去不溶性杂质后,用ZnO调节滤液使pH约等于2,加热、蒸发、浓缩制得较高温度下的硫酸锌饱和溶液,冷却结晶,得到粗制的硫酸锌晶体。
①加入少量氧化锌调节滤液使pH≈2目的是;
②加热蒸发、浓缩溶液时,应加热到时,停止加热。
(2)粗晶体在烧杯中用适量蒸馏水溶解,滴加1~2滴稀硫酸,用沸水浴加热至晶体全部溶解。停止加热,让其自然冷却、结晶。抽滤(装置如图所示)。将所得晶体用少量无水乙醇洗涤1-2次,得到较纯的硫酸锌晶体。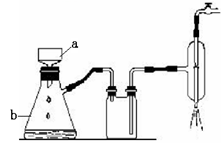
①写出下列仪器的名称。a ;b
②抽滤跟普通过滤相比,除了得到沉淀较干燥外,还有一个优点是。
③用少量无水乙醇洗涤晶体的目的是。
(3)在制取氢气时,如果锌粒中混有少量的铁、铜杂质,对硫酸锌的质量(填“有”、“无”)影响,原因是。