下列图示与对应的叙述相符的是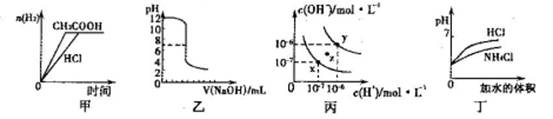
| A.甲图曲线表示向等体积、等物质的量浓度的盐酸和醋酸溶液中分别加人足量镁粉产生H2的物质的量的变化 |
| B.乙表示将0.01mol·L-lNaOH溶液滴人到稀盐酸中的滴定曲线 |
| C.丙为水的电离曲线,从z点到x点,可采用在水中加入适量NaOH固体的方法 |
| D.丁中曲线表示将pH相同的NH4C1溶液和盐酸稀释相同倍数时,二者pH的变化 |
将20 mL 10 mol·L-1的浓盐酸滴入盛有足量MnO2粉末的烧瓶中并加热,若不考虑HCl的挥发,则被氧化的氯化氢的物质的量是( )
| A.小于0.1 mol | B.等于0.1 mol |
| C.大于0.1 mol,小于0.2 mol | D.等于0.2 mol |
卤素原子之间可以形成类似卤素单质的分子,如溴化碘(IBr)能跟大多数金属反应生成金属卤化物,能跟水反应,其化学方程式为IBr+H2O====HBr+HIO。下面有关IBr的叙述中不正确的是 ( )
| A.在很多反应中IBr是强氧化剂 |
| B.IBr与H2O反应时,其氧化产物是HBr,还原产物是HIO |
| C.IBr跟NaOH溶液反应生成NaBr、NaIO和H2O |
| D.IBr跟金属锌反应生成ZnBr2和ZnI2 |
原子X转移一个电子给原子Y,形成化合物HY,下列说法正确的是()
| A.X被氧化了 | B.X是氧化剂 |
| C.X发生还原反应 | D.Y在反应中表现了氧化性 |
在室温条件下,保存下列药品的方法不正确的是()
| A.氢氧化钠用带玻璃塞的玻璃瓶保存 | B.保存液溴要加少量水形成液封 |
| C.硝酸银溶液装在棕色瓶中避光保存 | D.钠保存在煤油中 |
长期以来一直认为氟的含氧酸不存在,自1971年美国科学家用F2通过细冰来获得次氟酸(HFO)以来,对HFO的研究引起了充分重视。
(1)次氟酸能与水反应得到溶液A,A中含B、C两种溶质,B常用于雕刻玻璃,C在加热条件下分解生成一种能使带火星的木条复燃的气体(已知2H2O2 2H2O+O2↑),则次氟酸与水反应的化学方程式为。
2H2O+O2↑),则次氟酸与水反应的化学方程式为。
(2)写出在加热条件下F2(g)跟烧碱反应的化学方程式:。
(3)判断次氟酸中氧元素的化合价。