某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2- 中的若干种离子,离子浓度均为0.1 mol·L-1,某同学进行了如下实验:
下列说法正确的是
| A.无法确定原试液中是否含有Al3+、Cl- |
| B.滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+ |
| C.无法确定沉淀C的成分 |
| D.原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42- |
下图曲线a表示放热反应X(g)+Y(g) Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是()
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是()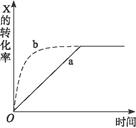
| A.升高温度 | B.加大X的投入量 | C.加催化剂 | D.增大体积 |
在恒温恒容条件下,能使A(g)+B(g) C(g)+D(g)正反应速率增大的措施是()
C(g)+D(g)正反应速率增大的措施是()
| A.减小C或D的浓度 | B.增大D的浓度 |
| C.减小B的浓度 | D.增大A或B的浓度 |
下图所示的直型石英玻璃封管中充有CO气体,左端放置不纯的镍(Ni)粉。在一定条件下,Ni可以与CO(g)发生如下反应:
Ni(s)+4CO(g) Ni(CO)4(g)
Ni(CO)4(g)
但Ni粉中的杂质不与CO(g)发生反应。玻璃管内左右两端的温度分别稳定在350 K和470 K,经过足够长时间后,右端的主要物质是()
| A.纯Ni(s)和Ni(CO)4(g) | B.纯Ni(s)和CO(g) |
| C.不纯Ni(s)和CO(g) | D.不纯Ni(s)和Ni(CO)4(g) |
哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生。下列有关说法正确的是()
| A.达到化学平衡时,N2将完全转化为NH3 |
| B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 |
| C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 |
| D.达到化学平衡时,正反应和逆反应的速率都为零 |
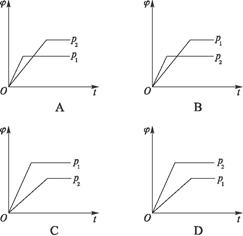
在一定温度不同压强(p1<p2)下,可逆反应2X(g) 2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系有以下图示,正确的是()
2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系有以下图示,正确的是()