明星化学兴趣小组就空气中氧气的含量进行实验探究.
【集体讨论】
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体。他们应该选择(填编号) .
| A.蜡烛 | B.红磷 | C.硫粉 | D.光亮的铁丝 |
为了充分消耗容器中的氧气,药品的用量应保证 .
(2)小组同学共同设计了如下图的两套装置,你认为合理的是(填编号) .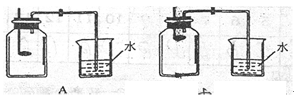
为了确保实验的成功,在装药品之前应该 .
【分组实验】
在讨论的基础上,他们分组进行了实验.
【数据分析】
实验结束后,整理数据见下表.(注:集气瓶容积为100 mL)
| 组 别 |
1 |
2 |
3 |
4 |
5 |
6 |
| 进入集气瓶中水的体积(mL) |
20 |
21 |
19 |
20 |
22 |
18 |
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的 .通过实验还可推断集气瓶中剩余气体的性质是 .
某课外小组研究“影响H2O2生成O2快慢的因素”的课题。通过查阅资料,他们提出如下猜想。
【提出猜想】催化剂和反应物浓度都会影响H2O2生成O2 的快慢
【实验过程】实验装置图如下: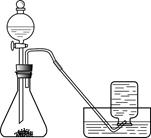
实验操作:检查装置气密性良好。将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体。
实验记录
| 实验编号 |
① |
② |
③ |
| 反应物 |
5%H2O2 100 mL |
5%H2O2 |
3%H2O2100 mL |
| 加入固体 |
0.5 g氯化钠固体 |
0.5 g二氧化锰 |
|
| 收集气体的时间 |
165 s |
46s |
80 s |
(1)H2O2溶液和二氧化锰制取氧气的化学方程式为 。
(2)实验②中加入H2O2的体积为 mL。
(3)实验③中加入的固体和用量为 。
【结论】该探究过程得出的结论是 。
【反思】H2O2在常温下分解缓慢,加入MnO2 后反应明显加快。小红提出,为了更好的证明二氧化锰和氯化钠是否对H2O2生成O2快慢有影响,还应该增加一组对比实验。该实验选用的药品和用量为 。
【实验拓展】小红用收集的气体进行氧气的性质实验。
(1)检验氧气的方法是 。
(2)小红发现用该气体进行氧气的性质实验,现象都不明显。造成这种结果的原因是 。
某校化学兴趣小组的同学设计实验验证红热的铁与水蒸气反应生成氢气,设计的实验装置图如下图。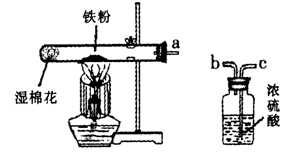
请回答下列问题。
(1)若干燥从a导管出来的气体,应从(选填“b”或“c”) 端管口通入。
(2)点燃生成的气体,产生色火焰。点燃前应进行的操作名称是。
(3)已知试管内湿棉花不参加化学反应,它的作用是。
(4)该小组同学用生成的氢气与氧化铁反应,反应的化学方程式是: 3H2 + Fe2O3 2Fe + 3H2O实验装置如右图。该实验观察到的现象有。
2Fe + 3H2O实验装置如右图。该实验观察到的现象有。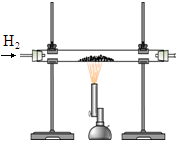
根据下图回答问题。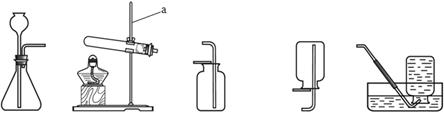
A BC D E
(1)实验仪器a的名称是。
(2)实验室用高锰酸钾制取氧气的化学方程式为,所选用的发生装置是(填字母序号,下同)。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气时,二氧化锰起作用。
(4)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_____。实验室制取氧气和制取二氧化碳都可选用的收集装置是_____。
轻质碳酸钙可用作牙膏摩擦剂。工业上常用石灰石(含有少量杂质)来制备比较纯净的轻质碳酸钙。
已知:①石灰石高温煅烧可以生成生石灰和二氧化碳,此外还有少量不反应的杂质剩余。
②生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆。
某实验小组同学设计了2种转化流程,如下图所示。
请回答下列问题:
(1)石灰石高温煅烧反应的化学方程式是。
(2)物质B为。
(3)反应④的化学方程式是。
(4)操作Ⅱ应采用的方法是。
(5)采用反应①②③制备轻质碳酸钙的方法优点有(写出一种即可);采用反应①②④制备轻质碳酸钙的方法优点有(写出一种即可)。
现有三种常见的矿石,分别是铁矿石、硫酸铜和石灰石中的一种。某化学兴趣小组对这三种矿石的成分产生兴趣,进行以下研究。请根据初中所学知识,回答下列问题:
(1)三种矿石中只有一种为白色固体,放入水中后不溶解,初步判断该矿石可能为。为了进一步证明,取少量该矿石于试管中,加入稀盐酸,产生大量气泡,该气体可使澄清石灰水变混浊。反应的化学方程式是、。
(2)第二种矿石放入水中,矿石逐渐溶解,并形成了蓝色溶液。向所得溶液中插入一根铁丝,一段时间后,铁丝上有红色物质析出,该反应的化学方程式为。
(3)第三种矿石的主要成分X由两种元素组成。已知120 g X和氧气充分反应,生成一种无色有刺激性气味的气体128 g,该气体会导致酸雨。X的化学式为。