15.有机电解制备的金属醇盐,可直接作为制备纳米材料的前体。以下是一种电化学合成金属醇盐的主要装置。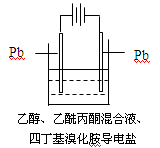
在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
2CH3CH2OH+2e-=2CH3CH2O-+H2↑
2CH3COCH2COCH3+2e—=2(CH3COCHCOCH3)+H2↑
下列说法正确的是
| A.阳极Pb失去电子,发生还原反应 |
| B.当阳极失去2 mol e—时,阴极产生2 mol氢气 |
| C.电解过程中,阳离子向阴极移动 |
| D.已知Pb-4e—=Pb4+,当消耗Pb的质量为103.5 g时,则转移电子2 mol |
下图是两种致癌物质的结构简式, 以下的描述正确的是
(1)苯并[a]芘(2)尼古丁
| A.(1)的分子式是 C20H12 |
| B.(2)的分子式是 C10H13N2 |
| C.它们都属于烃 |
| D.(1) 的分子是由5个苯的结构单元并合而成,所以它是苯的同系物 |
下列烃中可能存在同分异构体的是()
| A.丙稀 | B.乙烷 | C.丙烷 | D.丁烷 |
萘环上的碳原子的编号如(I)式,根据系统命名法,(II)式可称为2一硝基萘,则化合物 (III)的名称应是: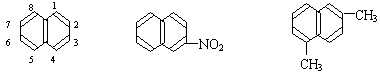
| A.2,6一二甲基萘 | B.2,5一二甲基萘 |
| C.4,7一二甲基萘 | D.1,6一二甲基萘 |
一种烃的结构式可以表示为: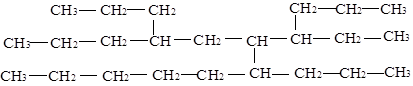
命名该化合物时, 主链上的碳原子数是
| A.9 | B.11 | C.12 | D.13 |
甲酸的结构如图 ,则它含有官能团的种数为
,则它含有官能团的种数为
| A.1种 | B.2种 | C.3种 | D.4种 |