去年冬天至今年春天,我国西南地区遭遇大范围持续干旱。全国人民团结一致,共同抗旱。
(1)有些村庄打深井取用地下水。检验地下水是硬水还是软水,可用的物质是 ,
(2)有些村民取浑浊的坑水作生活用水。有同学利用所学的知识将浑浊的坑水用右图所示的简易净水器进行净化,其中小卵石、石英沙的作用是 。
(3)如果地下水硬度大,或者坑水中病原微生物过多,都可以采取______ 方法,来降低硬度和杀灭病原微生物。
(4)身处旱区之外的我们能做些什么? (举一做法)
现有以下6个变化:
①在点燃的条件下,氢气在氧气中燃烧;
②给水通直流电
③锌加入稀硫酸溶液中;
④氢氧化钠溶液与稀盐酸混合
⑤冷却硝酸钾热饱和溶液析出硝酸钾晶体;
⑥日本福岛第一核电站发生核反应,铀235裂变产生碘131
请回答下列问题:
(1)探究化学变化的规律始终是化学科学的核心任务。上述变化中,属于化学变化的是(填变化的代号,下同)_______________,属于物理变化的是______________;
(2)化学变化也叫化学反应,在上述化学反应中,属于分解反应的有________________,属于复分解反应的有________________,将化学反应分为分解反应、化合反应、复分解反应和置换反应等四种基本反应类型的依据是_________________________、
(3)我们知道,能直接构成物质的微粒有分子、原子、离子。物质之所以发生化学反应,从微观的角度看,是因为反应物的微粒之间在一定条件下发生有效的相互作用,使微粒的结构发生改变,或微粒重新排列组合,宏观上表现为生成了新的物质。
在反应①中,发生有效相互作用的微粒是(写出微粒的符号)___________________。
反应的化学方程式为___________________________________________________
发生有效相互作用而促使反应发生的微粒是(写出微粒符号)__________________,微粒的转化过程是________________________________________________________________,
在反应④中,发生有效的相互作用而促使反应发生的微粒是(写出微粒的符号)____________
完成下列变化的化学方程式,并按要求填空。
(1)双氧水在二氧化锰催化下的反应:;其基本反应类型是。
(2)生石灰作干燥剂的反应:;它是(选填“吸热”或“放热”)反应。
(3)“湿法冶铜”的反应:;其基本反应类型是。
(4)中和反应(试举一例):;其基本反应类型是。
(5)金属镁着火不能用二氧化碳扑救,因为镁可以在二氧化碳中继续燃烧生成氧化镁和单质:。
利用工业煤制乙二醇(重要的化工原料),因具有低成本、低能耗、低排放等特点而具有非常广阔的前景,该制备过程如图所示。回答下列问题:
(1)“造气”过程的微观示意图如下,则制备合成气的化学方程式为。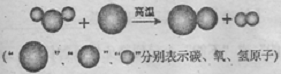
(2)合成气有还原性,可用于冶炼钢铁。请写出合成气与Fe2O3反应的一个化学方程式:。
(3)合成气在不同催化剂作用下,可以合成不同的物质。仅用合成气为原料不可能得到的物质是(填字母序号)。
A、草酸(HOOCCOOH) B、甲醇(CH3OH) C尿素[CO(NH2)2]
(4)从煤直接作燃料到用煤制取乙二醇,你得到的启示是。
硫铁矿(主要含FeS2)是工业制硫酸(H2SO4)的原料,第一步在高温下将硫铁矿的粉末与氧气充分反应生成氧化铁和二氧化硫,再经过一系列转化生成硫酸。第一步的反应可用化学方程式表示为: 4FeS2+xO2==2Fe2O3+ySO2(x、y表示化学计量数),则其中的x= 。
实验室中,利用下列装置可以制取某些气体,请回答下列问题。
(1)向气体发生装置内加入药品前,应该进行的操作是。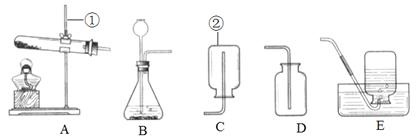
(2)实验室若用高锰酸钾制取氧气,选择的发生装置是。
(3)乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取乙炔应选择的发生装置是;收集装置是。