下列有关物质的性质、应用等说法正确的是
| A.SiO2既能溶于NaOH溶液又能溶于HF溶液,说明SiO2是两性氧化物 |
| B.将铜片放入冷的浓硫酸中,无明显现象,说明铜在浓硫酸中发生了钝化 |
| C.浓硫酸能干燥SO2等气体,说明浓硫酸具有吸水性 |
| D.自来水厂可用明矾对水进行消毒杀菌 |
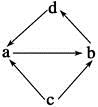
下列各组物质中,物质之间通过一步反应就能实现图示变化的是
| 物质编号 |
物质转化关系 |
a |
b |
c |
d |
| ① |
 |
FeCl2 |
FeCl3 |
Fe |
CuCl2 |
| ② |
NO |
NO2 |
N2 |
HNO3 |
|
| ③ |
Na2O |
Na2O2 |
Na |
NaOH |
|
| ④ |
Al2O3 |
NaAlO2 |
Al |
Al(OH)3 |
A.①④B.①②③C.①③④ D.②④
有A、B、C、D、E和F六瓶无色溶液,它们都是中学化学中常用的无机试剂。E的溶质是一种无色油状液体;B、C、D和F是盐溶液,且它们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;②将A分别加入其他五种溶液中,只有D、F中有沉淀产生,继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。根据上述实验信息,下列说法错误的是
A.B可能是NaHCO3溶液
B.F为AgNO3溶液
C.D不可能是镁或铝的盐酸盐
D.A为氨水,E为硫酸
下列类比关系正确的是
| A.钠与氧气在不同条件下反应会生成两种不同的氧化物,则Li与氧气反应也能生成Li2O或Li2O2 |
| B.Na2O2与CO2反应生成Na2CO3和O2,则Na2O2与SO2反应可生成Na2SO3和O2 |
| C.Fe与Cl2反应生成FeCl3,则Fe与I2反应可生成FeI3 |
| D.Al与Fe2O3能发生铝热反应,则Al与MnO2也能发生铝热反应 |
将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是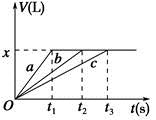
| A.x=2.24 |
| B.钠的物质的量为0.2 mol |
| C.反应时,Na、Mg、Al均过量 |
| D.曲线b为Mg与盐酸反应的图像 |
海水是重要的资源。可以制备一系列物质
下列说法正确的是
| A.步骤②中,应先通CO2,再通NH3 |
| B.步骤③可将MgCl2·6H2O晶体在空气中直接加热脱水 |
| C.步骤④、⑤、⑥反应中,溴元素均被氧化 |
D.除去粗盐中的 、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸 、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸 |