短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是形成酸雨的主要物质之一。
| X |
|
|
|
| Z |
|
W |
Y |
(1)写出W的原子结构示意图: 。
(2)已知:
①X(s) + O2(g) =XO2(g) ΔH=-393.5 kJ·mol-1
②H2(g) + 1/2 O2(g) =H2O(g) ΔH=-242.0 kJ·mol-1
③XH4(g) + 2O2(g) =XO2(g) + 2H2O(g) ΔH=-802.0 kJ·mol-1
则XH4气体分解成氢气和X固体的热化学方程式为 。
(3)ZO是由单质X和ZO2反应制取单质Z的中间产物(空气中极不稳定)。隔绝空气时,ZO与NaOH溶液反应(产物含有一种固体单质和一种钠盐)的化学方程式为__________________________。
(4)元素Y的Ca盐和H2为原料,反应产物只有甲和乙两种且均为化合物。研究发现:化合物甲的组成中钙、元素Y的质量分数分别为52.29%、46.41%;化合物乙的水溶液显酸性。则乙的化学式为 ;甲与水反应可得H2,其化学方程式是: 。
(5)将W的气态氢化物通入一定量的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,生成气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。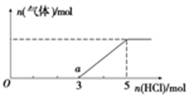
①O点溶液中所含溶质的化学式为____________。
②a点溶液中,c(Na+):c(Cl-)= _______________。
(1)苯、四氯化碳、乙醇都是常见的有机溶剂。能与水互溶的是 ;难溶于水,且密度比水小的是 。
(2)一瓶无色气体,可能含有CH4和CH2 CH2,也可能是其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有无色油状小液滴。
CH2,也可能是其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有无色油状小液滴。
①由上述实验现象推断出该混合气体中一定含有CH4,你认为是否正确,说明理由。
____________________________________
②上述实验过程中可能涉及的反应类型有:_____________
下图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合。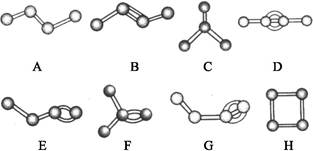
(1)图中属于烷烃的是 。(填编号)
(2)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成碳碳单键,还可以形成 和 ;不仅可以形成 ,还可以形成碳环。
(3)上图中互为同分异构体的是:A与 ;B与 ;D与 。(填编号)
已知化学能与其他形式的能可以相互转化。填写下表的空白:
| 化学反应方程式(例子) |
能量转化形式 |
| ① |
由化学能转化为热能 |
②Pb+PbO2+2H2SO4 2PbSO4+2H2O 2PbSO4+2H2O |
|
③CaCO3 CaO+CO2↑ CaO+CO2↑ |
上述反应中属于氧化还原反应的是(填序号) 。
选择适宜的材料和试剂设计一个原电池,完成下列反应:
Zn+CuSO4=ZnSO4+Cu
(1)画出装置图,并标明各部分材料名称。
(2)负极材料 ,正极材料 ,电解质溶液是 。
(3)写出电极反应式:
负极: _______________________
正极: _______________________
298 K时,合成氨反应:N2(g)+3H2(g) 2NH3(g),生成2 mol NH3放出92.4 kJ热量。在该温度下,取1 mol N2(g)和3 mol H2(g)在密闭容器中充分反应,放出的热量 (填“等于”“大于”或“小于”)92.4 kJ。原因是 _____________________________
2NH3(g),生成2 mol NH3放出92.4 kJ热量。在该温度下,取1 mol N2(g)和3 mol H2(g)在密闭容器中充分反应,放出的热量 (填“等于”“大于”或“小于”)92.4 kJ。原因是 _____________________________