下列说法错误的是()
| A.化学反应实质是旧键断裂和新键形成 |
| B.极性键就是共用电子对发生偏移的共价键 |
| C.氢键是一种比较弱的化学键 |
| D.水结冰时体积膨胀、密度减小就是因为氢键的存在 |
在一定条件下,反应N2+3H2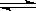 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为()
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为()
| A.V(NH3)=0.02mol/(L·min) | B.V(N2)=0.005mol/(L·min) |
| C.V(NH3)=0.17mol/(L·min) | D.V(H2)=0.03mol/(L·min) |
等质量的下列烃完全燃烧,消耗氧气最多的是()
| A.CH4 | B.C2H4 | C.C4H8 | D.C6H6 |
用于制造隐形飞机的某物质具有吸收微波的功能,其主要成分的结构如图,它属于()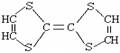
| A.无机物 | B.烃 | C.高分子化合物 | D.有机物 |
巴豆酸的结构简式为CH3—CH=CH—COOH。现有①氯化氢、②溴水、③纯碱溶液、④乙醇、⑤酸性高锰酸钾溶液,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是()。
| A.只有②④⑤ | B.只有①③④ | C.只有①②③⑤ | D.①②③④⑤ |