(每空2分,共16分).下图中的A、B、C、D、E、F、G均为有机物
据上图回答问题:
(1)D的化学名称是 。
(2)G与溴水反应的化学方程式是 (有机物须用结构简式表示)。
(3)B的分子式是: A的结构简式是 ①反应的反应类型是 。
(4)符合下列3个条件的B的同分异构体的数目有 个
(ⅰ)含有邻二取代苯环结构
(ⅱ)与B有相同官能团
(ⅲ)不与FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式 。
(5)G是的工业原料,用化学方程式表示G的一种的工业用途 。
实验室里一些看似简单的基本操作往往需要方法或技巧,下表中A栏列出操作的要求或目的,请在对应B栏中填上方法或技巧:
| 序号 |
A |
B |
| ① |
用滴管从试剂瓶中吸取液体 |
|
| ② |
让往玻璃导管套上橡皮管容易些 |
|
| ③ |
为使加热的蒸发皿里的液体不溅出 |
|
| ④ |
往大试管里加入颗粒状锌 |
|
| ⑤ |
实验室保存液溴,避免液溴挥发掉 |
将32 g Cu与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
(1)NO的物质的量为 mo
mo L,NO2的物质的量为 moL。
L,NO2的物质的量为 moL。
(2)产生的气体全部释放后,向溶液中加入V mL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的浓度为mol/L。
(3)欲使铜与硝酸 反应生成的气体在氢氧化钠溶液中全部转化为NaNO3,至少需要质量分数为30%的双氧水g。
反应生成的气体在氢氧化钠溶液中全部转化为NaNO3,至少需要质量分数为30%的双氧水g。
已知A、B、C、D的组成元素都属于短周期,其中A、D为单质,B、C为化合物,它们之间的简单转化关系如图所示。请按要求写出有关反应式,是离子反应的只写离子方程式: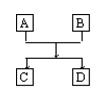
(1)若A、D的组成元素同主族:
①B是水:__________________________________________。
②B、C均为氧化物(反应有重要的工业价值):
____________________________________________。
(2)若A、D的组成元素不同主族:
①B是水且水是还原剂:__________________________________________;
B是水且水是氧化剂(反应有重要的工业价值): ___________ __________。
__________。
②B、C均为氧化物:____________________________________________。
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:
CO(g)+2H2(g) CH3OH(g);△H
CH3OH(g);△H
下图表示某次合成实验过程中甲醇的体积分数 φ(CH3OH)与反应温度的关系曲线,若在230℃时,平衡常数K=1。若其它条件不变,将温度升高到500℃时,达到平衡时,K1 (填“>、< 或 = ”)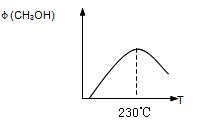
(2)利用甲醇燃料电池设计如下图所示的装置:则该装置中Cu极为极;写出b极的电极反应式 ,当铜片的质量变化为12.8 g时:a极上消耗的O2在标准状况下的体积为 L。
L。 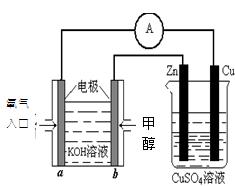
| 难(微)溶物 |
溶度积常数(Ksp) |
BaSO 4 4 |
1×10-10 |
| BaCO3 |
2.6×10-9 |
| CaSO4 |
7×10-5 |
| CaCO3 |
5×10-9 |
(3)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。
具体做法是用饱和纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.0lmol·L-1以上,则溶液中CO32-物质的量浓度应≥
 mol·L-1
mol·L-1
某实验室把学生做完实验后的废液(含氯化钠、氯化铁、氯化铜等)进行集中处理,过程如下: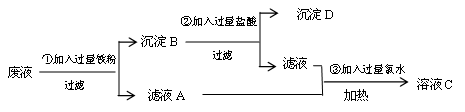
(1)沉淀D的化学式为。
(2)反应③中Cl2属于(填“氧化剂”或“还原剂”)。
(3)写出①反应中的离子方程式
。
(4)溶液C中的溶质是(提示:加热后,溶液中没有了HCl和Cl2),若要进一步进行分离,方法是。