将6 g 铁粉加入200 mL Fe2(SO4)3和CuSO4的混合溶液中,充分反应得到200 mL 0.5 mol /L FeSO4溶液和5.2 g固体沉淀物。试计算:
(1)反应后生成铜的质量;
(2)原Fe2(SO4)3溶液的物质的量浓度。
用足量的NaOH吸收448mLCl2(标准状况)氯气,计算生成NaCl的物质的量。
某课外兴趣小组对H2O2的分解速率做了如下实验探究。
⑴ 下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mLO2所需的时间(秒)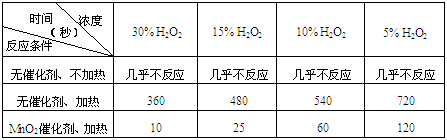
① 该小组在设计方案时,考虑了浓度、a: 、b: 等因素对过氧化氢分解速率的影响。
② 从上述影响H2O2分解速率的因素a和b中任选一个,说明该因素对该反应速率的影响:
。
⑵ 将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木
条测试。测定结果如下:
| 催化剂(MnO2) |
操作情况 |
观察结果 |
反应完成所需的时间 |
| 粉末状 |
混合不振荡 |
剧烈反应,带火星的木条复燃 |
3.5分钟 |
| 块状 |
反应较慢,火星红亮但木条未复燃 |
30分钟 |
① 写出H2O2发生的化学反应方程式 _______________ ______。
② 实验结果说明催化剂作用的大小与________ _________有关。
某含氧有机物的相对分子质量为60,1 mol该有机物完全燃烧,生成36gH2O和44.8L CO2(标准状况下)。
(1)求该有机物分子式;
(2)又知此有机物具有弱酸性,能与金属钠反应,也能与碱溶液反应,试写出它可能的结构简式。
现有22g Mg、Al、Zn、Fe多种活泼金属粉末的混合物与200mL含有一定质量的20%硫酸溶液恰好完全反应,得到无水盐70g,求(要求写出计算过程)
(1)硫酸溶液的质量?
(2)生成的气体体积(标准状况)?
(3)硫酸物质的量浓度?
溴水在科学实验中具有重要的作用,如可用于物质的鉴别和分离提纯。将6.72L(标准状况)乙烯和甲烷的混合气通入足量的溴水中,充分反应后,溴水的质量增加了1.4g,请列式计算原混合气体中乙烯和甲烷的物质的量之比是多少?