向盛有稀BaCl2(aq)的甲、乙两试管中分别通入SO2至饱和,若向甲试管中加入足量HNO3(aq),向乙试管中加入足量NaOH(aq)。则下列叙述正确的是
| A.甲、乙两试管中都有白色沉淀生成 |
| B.甲、乙两试管中都没有白色沉淀生成 |
| C.甲试管中没有白色沉淀生成,而乙试管中有 |
| D.乙试管中没有白色沉淀生成,而甲试管中有 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g) = CO2(g)+3H2(g);DH =" +" 49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g) = CO2(g)+2H2(g);DH =-192.9 kJ·mol-1
下列说法正确的是( )
| A.CH3OH(g)+3/2O2(g) = CO2(g)+2H2O(g);DH =-192.9 kJ·mol-1 |
B.反应①中的能量变化如图所示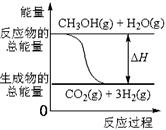 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应:CH3OH(l)+1/2O2(g) = CO2(g)+2H2(g)的△H>-192.9 kJ·mol-1 |
把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上有大量气泡产生,则四种金属的活动性顺序由强到弱为
| A.a>b>c>d | B.a>c>d>b | C.c>a>b>d | D.b>d>c>a |
下列各组物质中,所含化学键类型相同的是
| A.NaF、HNO3 | B.CO2、CH4 | C.HCl、MgF2 | D.Na2O、H2O |
甲、乙两种非金属元素:
①甲单质比乙单质容易与氢气化合
②甲元素的单质能与乙的阴离子发生氧化还原反应
③甲的最高价氧化物对应水化物的酸性比乙的最高价氧化物对应水化物的酸性强
④与某金属反应时,甲比乙得电子数多
⑤甲的单质熔沸点比乙的单质低。能说明甲比乙的非金属性强的是
| A.只有③④ | B.只有①②⑤ | C.只有①②③ | D.①②③④⑤ |
将过量的CO2通入下列溶液中,最终有沉淀的是
| A.CaCl2溶液 | B.石灰水 | C.Ca(ClO)2溶液 | D.Na2SiO3溶液 |