氢氟酸(HF)是一种弱酸。25℃时,向20mL0.1mol/L氢氟酸中加入VmL 0.1mol/LNaOH溶液充分反应。已知:
HF(aq)+OH-(aq)=F-(aq)+H2O(l) △H=-67.7kJ/mol
H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol
根据题意,下列判断或结论正确的是
| A.氢氟酸的电离过程是吸热的 |
| B.当V=20时,溶液中:c(F-)<c(Na+)=0.1mol/L |
| C.当V<20时,溶液中离子浓度关系可能为:c(Na+)=c(F-) |
| D.当V>20时,溶液中离子浓度关系一定为:c(Na+)>c(F-)>c(OH-)>c(H+) |
下列化学用语正确的是( )
A.CO2的电子式: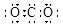 |
B.乙醛的结构简式:CH3COH |
C.甲烷分子的比例模型 |
D.6个中子的碳原子的核素符号12C |
除去Na2CO3溶液中少量NaHCO3溶液的最佳方法是
| A.加入适量盐酸 | B.加入NaOH溶液 |
| C.加热 | D.配成溶液后通入CO2 |
下列反应,其产物的颜色按红、红褐、淡黄、蓝色顺序排列的是
①金属钠在纯氧中燃烧;
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间;
③FeCl3溶液中滴入KSCN溶液;
④无水硫酸铜放入医用酒精中。
| A.②③①④ | B.③②①④ | C.③①②④ | D.③④①② |
将铁的化合物溶于盐酸,滴加KSCN溶液不发生颜色变化,再加入适量氯水,溶液立即呈红色的是
| A.Fe2O3 | B.FeCl3 | C.Fe2(SO4)3 | D.FeO |
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关。下列各组物质:
①Cu与HNO3溶液 ②Cu与FeCl3溶液
③Zn与H2SO4溶液 ④Fe与HCl溶液
由于浓度不同而能发生不同氧化还原反应的是( )
| A.①③ | B.③④ | C.①② | D.①③④ |