金属铬和氢气在工业上都有重要的用途。已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。

(1)铜铬构成原电池如右图1,其中盛稀硫酸烧杯中的现象为: 。盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是:
| A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液 |
| B.理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池 |
| C.此过程中H+得电子,发生氧化反应 |
| D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中 |
(2)如构成图2电池发现,铜电极上不再有图1的现象,铬电极上产生大量气泡,遇空气呈红棕色。写出正极电极反应式: 。
(3)某同学把已去掉氧化膜的铬片直接投入氯化铜溶液时,观察到了预料之外的现象:①铬片表面上的铜没有紧密吸附在铬片的表面而是呈蓬松的海绵状;②反应一段时间后有大量气泡逸出,且在一段时间内气泡越来越快,经点燃能发出爆鸣声,证明是氢气。请解释这两种现象的原因___________。
(1)已知:
① 2H2(g)+O2(g)=2H2O(l) △H1=" -a" kJ•mol-1
② 2CO(g)+O2(g)=2CO2(g) △H2 =" -b" kJ•mol-1
③ CO(g)+2H2(g) CH3OH(g) △H3 =" -c" kJ•mol-1
CH3OH(g) △H3 =" -c" kJ•mol-1
计算甲醇蒸气的标准燃烧热 =
=
(2)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,钴氧化物可通过处理钴渣获得。
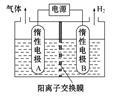
①利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为 溶液(填化学式),阳极电极反应式为 ,电解过程中Li+向 电极迁移(填“A”或“B”)。
②利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下: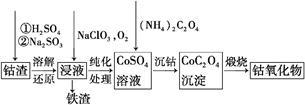
Co(OH)3溶解还原反应的离子方程式为 。
(1)砷(As)与其化合物被广泛应用在农药、除草剂、杀虫剂以及含砷药物中。回答下列问题:
①砷是氮的同族元素,且比氮多2个电子层,砷在元素周期表中的位置: ;AsH3的热稳定性比NH3的热稳定性 (填“强”或“弱”)。
②As2O3俗称砒霜,As2O3是两性偏酸性氧化物,是亚砷酸(H3AsO3)的酸
酐,易溶于碱生成亚砷酸盐,写出As2O3与足量氢氧化钠溶液反应的离子
方程式 。
③As2S3和HNO3反应如下:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O,将该反应设计成原电池,则NO2应该在 (填“正极”或“负极”)附近逸出,该极的电极反应式为 。
(2)综合利用CO2对环境保护及能源开发意义重大。Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是 。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 |
K+ NA+ Cu2+ Al3+ |
| 阴离子 |
SO42- HCO3- OH-Cl- |
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸酸化的硝酸钡溶液,只有A中放出无色气体,只有D中产生白色沉淀;
⑤将B、C两溶液混合,未见沉淀或气体生成。根据上述实验填空:
(1)写出B、D的化学式:B ____,D 。
(2)C可用作净水剂,用离子方程式表示其净水原理____ ___。
(3)将含0.01 mol A的溶液与含0.02 mol E的溶液反应后,向溶液中滴加0.1 mol·L-1稀盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是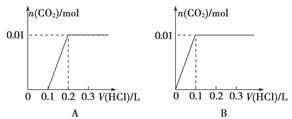
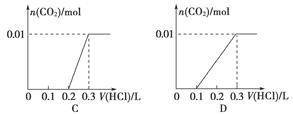
(4)在m mL B mol·L-1 C溶液中,加入等体积A mol·L-1的E溶液。当A≤3B时,生成沉淀的物质的量是 mol;当3B<A<4B件时,生成沉淀的物质的量是 mol。
某工业废水中可能含有如下几种阴阳离子:
| 阳离子 |
Fe3+、Al3+、Fe2+、Ba2+、Na+ |
| 阴离子 |
Cl-、CO32-、NO3-、SO42-、SiO32- |
现对该废水样品进行以下研究:
Ⅰ.取少量的废水于试管中,观察颜色,嗅气味,与普通水明显不同;
Ⅱ.向试管中滴加浓盐酸,有少量的无色气体生成,气体遇空气立即变为红棕色;
Ⅲ.若向II所得的溶液中加入BaCl2溶液,有白色沉淀生成;
Ⅳ.若向II所得的溶液中加入过量的NaOH溶液,有红褐色沉淀生成。过滤后向所得滤液中通入过量的CO2气体,有白色絮状沉淀生成。
根据上述实验,回答下列问题:
(1)该废水中一定含有的阴离子是 ,一定不含有的阳离子是 ;
(2)写出IV的所得滤液中通入过量的CO2气体生成白色絮状沉淀的离子方程式(只写这一个): ;
(3)若将废水中的铁元素完全转化成Fe3+,此时测得c(Fe3+)=1.0×10-2mol·L-1,要想将其转换为Fe(OH)3沉淀而除去,则应调节溶液pH约为 。(已知常温下Fe(OH)3的Ksp=1.0×10-38)
蓄电池是一种反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应如下:NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)此蓄电池在充电时,电池负极应与外加电源的_____极连接,电极反应式为_____________。
(2)以铜为电极,用此蓄电池作电源,电解以下溶液,开始阶段发生反应:
Cu+2H2O===Cu(OH)2+H2↑的有______________。
| A.稀H2SO4 | B.NaOH溶液 | C.Na2SO4溶液 | D.CuSO4溶液 E.NaCl溶液 |
(3)假如用此蓄电池电解以下溶液(电解池两极均为惰性电极),工作一段时间后,蓄电池内部消耗了0.36 g水。试回答下列问题:
①电解足量N(NO3)x溶液时某一电极析出了a g金属N,则金属N的相对原子质量R的计算公式为R=____________(用含a、x的代数式表示)。
②电解含有0.1 mol·L-1的CuSO4溶液100 mL,阳极产生标准状况下的气体体积为________L;将电解后的溶液加水稀释至2L,溶液的pH=_____。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质、CH4为燃料、空气为氧化剂、稀土金属材料为电极的新型电池。已知该熔融盐电池的负极的电极反应是:CH4-8e-+4 CO=5CO2+2H2O,则正极的电极反应式为_______________________。
(5)有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH=-a kJ·mol-1;
CH3OH(g)===CH3OH(l) ΔH=-b kJ·mol-1;
2H2(g)+O2(g)===2H2O(g)ΔH=-c kJ·mol-1;
H2O(g)===H2O(l) ΔH=-d kJ·mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为 。