下列实验操作错误的是
| A.用蒸馏的方法分离汽油和煤油 |
| B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C.浓硫酸稀释时,应将浓硫酸慢慢加到水中,及时搅拌并冷却 |
| D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2 |
pH=1的两种一元酸HX和HY溶液,分别取100mL加入足量的镁粉,充分反应后,收集到H2体积分别为VHX和VHY。若相同条件下VHX>VHY,则下列说法正确的 ()
| A.HX可能是强酸 | B.HY一定是强酸 |
| C.HX的酸性强于HY的酸性 | D.反应开始时二者生成H2的速率相等 |
在下图各烧杯中盛有海水,铁在其中腐蚀速率由快到慢的顺序是()。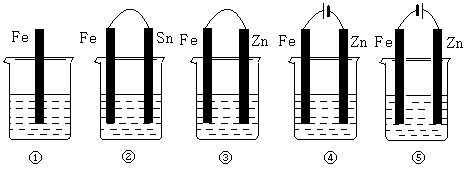
| A.①>②>③>④>⑤ | B.⑤>④>③>②>① |
| C.④>②>①>③>⑤ | D.②>③>⑤>①>④ |
已知0.02 mol·L-1CH3COOH溶液和0.01 mol·L-1NaOH溶液以等体积混和后溶液呈酸性,则该混合液中微粒浓度关系正确的 ( )
| A.c (CH3COO-)>c (Na+) |
| B.c (Na+) + c (H+) =c (OH-) +c (CH3COOH)+c (CH3COO-) |
| C.c (CH3COOH)>c (CH3COO-) |
| D.c (CH3COOH)+c (CH3COO-)="0.02" mol·L-1 |
某密闭容器中发生如下反应:X(g)+3Y(g)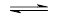 2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是()
2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是()
| A.t5时增大了压强 |
| B.t3时降低了温度 |
| C.t2时加入了催化剂 |
| D.t4~t5时间内转化率一定最低 |
对室温下pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是 ()
| A.加适量的醋酸钠晶体后,两溶液的pH均增大 |
| B.使温度都升高20℃后,两溶液的pH均不变 |
| C.加水稀释2倍后,两溶液的pH均减小 |
| D.加足量的锌充分反应后,两溶液中产生的氢气一样多 |