(本题共2小题,共10分)
(1)相同温度下等物质量浓度的下列溶液中,
| A.NH4Cl | B.NH4HCO3 | C.NH4HSO4 | D.(NH4)2SO4 |
①pH值由大到小的顺序是 (用对应的字母填写)。
②NH4+离子浓度由大到小的顺序是 (用对应的字母填写)。
③若上述溶液的pH值相同,则其物质的量浓度关系是 (用对应的字母填写)。
(2)向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.020 mol·L-1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10-10,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中c(Ag+)=________。
②完全沉淀后,溶液的pH=________。
(15分)已知A、B、C、D、E、F是原子序数依次增大的短周期主族元素。A的最外层电子数等于其电子层数,B元素形成的化合物种类最多,D是地壳中含量最高的元素,D和E同主族。Q是第四周期元素,最外层只有一个电子,其余各层电子均充满。
请回答下列问题(用元素符号或化学式表示):
(1)元素B、C、D的电负性由大到小的顺序是 。
(2)A3D+的中心原子杂化轨道类型是 ,该离子的立体构型是 。
(3)向QF2的水溶液通入ED2,产生白色沉淀QF,该反应的化学方程式是 。
(4)一种处理汽车尾气中CD、BD2的方法是在催化剂作用下使两者反应成无污染的气态。已知反应生成1g C的单质时放出4.3kJ热量。此反应的热化学方程式为 。
(5)Q+的核外电子排布式为 ,下图是由C、Q形成的某种化合物的晶胞结构示意图,该晶体的化学式 ;C的配位数为 。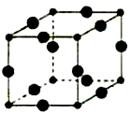
(6)C2A4 ─ 空气燃料电池是一种碱性燃料电池。电解质溶液是20%~30%的KOH溶液。则燃料电池放电时:负极的电极反应式是 。
(1)(5分)由A、B两种气态烃组成的混合气体,对H2的相对密度为17。常温常压下,取这种混合气体10mL与80mL氧气(过量)混合,当完全燃烧后恢复到原状态时,测得气体的体积为70mL。试求:
①混合气体的平均组成为(用CxHy的形式表示)___________;
②若上述两种气体按体积1:1混合时,则两种气态烃的可能组成为__________________。
(2)(5分)具有支链的化合物X的分子式为C4H8O,X既能使Br2的四氯化碳溶液褪色,又能与Na反应。①X的结构简式是,
②写出与X具有相同官能团的X的所有同分异构体的结构简式:______________。
(1)请写出下列物质的结构简式:
①2-甲基-3-乙基戊烷:;
②2,3-二甲基-1-丁烯:。
(2)请写出下列物质的名称:
(3)在有机反应中,反应条件尤为重要。条件(如温度、溶剂、催化剂等)改变,反应产物可能会随之改变。
①已知苯与浓硝酸、浓硫酸的混合物在50-60℃反应时生成硝基苯;若反应条件升温至100-110℃时,反应的化学方程式为。
②卤代烃与碱反应时,溶剂不同则产物不同。若溴乙烷与氢氧化钾的水溶液反应,反应的化学方程式为:。
③甲苯能与溴蒸汽在光照条件下发生反应生成一溴代物,反应的化学方程式为:。
(4)某有机分子结构如下:
该分子中至少有个C原子在同一平面,最多有个C原子在同一平面。
已知A、B、C、D、E、F、G都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素。A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子,G的+1价阳离子正好充满K、L、M三个电子层。回答下列问题:
(1)A、B、C、D、E、F、G几种元素中第一电离能最小的是___________(填元素符号),D元素的原子核外有种不同运动状态的电子;有种不同能级的电子。基态的F3+核外电子排布式是。
(2)B的气态氢化物在水中的溶解度远大于A、C的气态氢化物,原因是。
(3)化合物AC2的电子式是。
(4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是。
(5)化合物EF[F(AB)6]是一种蓝色晶体,下图表示其晶胞的1/8(E+未画出)。该蓝色晶体的一个晶胞中E+的个数为。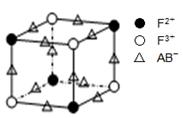
(6)G的二价阳离子能与乙二胺(H2N—CH2一CH2一NH2)形成配离子:该配离子中含有的化学键类型有。(填字母)
a.配位键 b.极性键 c.离子键 d.非极性键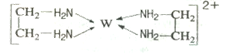
阴离子CAB-中的A原子与乙二胺(H2N—CH2一CH2一NH2)中C原子的杂化方式分别为和。
石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。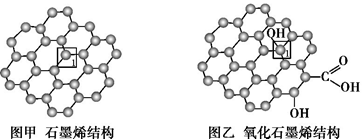
(1)图甲中,1号C与相邻C形成σ键的个数为 。
(2)图乙中,1号C的杂化方式是 ,该C与相邻C形成的键角 (填“>”“<”或“=”)图甲中1号C与相邻C形成的键角。
(3)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有 (填元素符号)。
(4)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一 种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部。该晶胞中M原子的个数为 ,该材料的化学式为 。