下列事实得出的结论正确的是
| A.可用加热法除去氯化钠固体中的氯化铵杂质 |
| B.只用铜片不能鉴别浓硝酸和稀硝酸 |
| C.常温下,Al和浓硫酸钝化说明Al和浓硫酸在常温下不反应 |
| D.SO2通入氯化钡溶液无现象,若再通入NH3或NO2气体则都会产生BaSO4的白色沉淀 |
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ |
| C.向反应后的溶液加入乙醇,溶液没有发生变化 |
| D.在[Cu(NH3)4]2+离子中,Cu2+提供孤电子对,NH3提供空轨道 |
短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是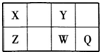
| A.钠与W可能形成Na2W2化合物 |
| B.由Z与Y组成的物质在熔融时能导电 |
| C.W得电子能力比Q强 |
| D.X有多种同素异形体,而Y不存在同素异形体 |
根据键能数据估算CH4 (g)+4F2 (g) =CF4+4HF(g)的反应热ΔH为
| 化学键 |
C—H |
C—F |
H—F |
F—F |
| 键能/(kJ/mol) |
414 |
489 |
565 |
155[ |
A.–1940 kJ · mol-1B.+1940 kJ · mol-1
C.–485 kJ · mol-1D.+485 kJ · mol-1
用价层电子对互斥理论(VSEPR)预测H2S和COCl2的立体结构,两个结论都正确的是
| A.直线形;三角锥形 | B.V形;三角锥形 |
| C.直线形;平面三角形 | D.V形;平面三角形 |
下列说法中错误的是
| A.根据对角线规则,铍和铝的性质具有相似性 |
| B.在H3O+、NH4+和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.P4和CH4都是正四面体分子且键角都为109o28ˊ |