(6分)下表为各物质中所含有的少量杂质,在空格处填写除杂所用试剂和操作方法。
| 序号 |
物质 |
杂质 |
除杂质试剂 |
操作方法 |
| ① |
Fe(OH)3胶体[ |
Na+、Cl- |
水 |
|
| ② |
FeSO4溶液 |
CuSO4 |
|
|
| ③ |
CO2 |
HCl |
|
洗气 |
| ④ |
NaCl溶液 |
I2 |
|
|
某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
【提出假设】假设1:白色物质是Na2O。
假设2:白色物质是Na2CO3。
假设3:(请你写出)。
【设计实验方案、验证假设】该小组对燃烧后的白色产物进行如下探究:
| 实验方案 |
实验操作 |
实验现象 |
结论 |
| 方案1 |
取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 |
溶液变成红色 |
白色物质为Na2O |
| 方案2 |
①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 |
出现白色沉淀 |
(此处不要求填写) |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 |
无明显现象 |
【思考与交流】
(1)甲同学认为方案1得到的结论不正确,其理由是。
(2)通过方案1和方案2的实验,你认为上述三个假设中,成立。你的理由是。
(3)钠在二氧化碳中燃烧的化学方程式为。
(4)乙同学认为白色物质有可能是氢氧化钠 。你是否同意乙同学的观点,并简述由:。
。你是否同意乙同学的观点,并简述由:。
已知:
从A出发,发生下列图示的一系列反应,其中W和Z互为同分异构体。
请回答下列问题:
(1)写出反应类型:①,②。
(2)写出化学反应方程式:
③。
④。
(3)与  互为同分异构体,属于酚类且苯环上只有两个互为对位取代基的化合物共有4种,其结构简式
互为同分异构体,属于酚类且苯环上只有两个互为对位取代基的化合物共有4种,其结构简式
为: ,,。
,,。
(4)A的结构简式可能有种,请写出其中化学式不同的两种结构简式,。
某同学查阅资料得知,①草酸晶体(H2C2O4·2H2O)在175℃时受热分解,同时熔化且熔融时易挥发。②草酸晶体易溶于水,而草酸钙难溶于水。
为验证草酸分解的产物,该同学选择如下仪器和试剂中的部分完成此实验。
(1)草酸晶体受热分解的方程式为。
(2)草酸晶体受热分解时,选择的装置为,理由是。
(3)若只验证CO2气体一种产物时,除气体发生装置外所选择装置的接口顺序为。
(4)若验证所有的产物时,除气体发生装置外所选择的必要装置的接口顺序为。
(5)草酸晶体使酸性高锰酸钾溶液褪色的化学方程式为。
某同学利用乙烷燃料电池进行电解实验,如图所示: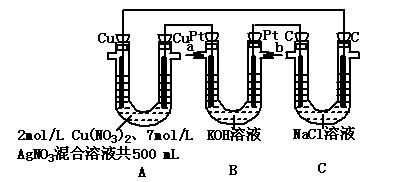
(1)一段时间后C装置的右侧碳棒附近有黄绿色气体逸出,则B装置中通入a气体为。
(2)B装置右侧电极的电极反应式为。
(3)C装置中左侧电极的电极反应式为,该极区的产物为。
(4)当A装置中的溶液质量不再变化,B装置中理论上消耗乙烷的质量为g。
(5)当A装置中溶液的质量不再变化,仍电解一段时间,若不考虑溶液体积的变化,此时溶液中溶质的物质的量浓度为mol/L。
已知A、B、C、D、E为周期表里1~20号元素中的五种。又知:①A与D同族,且A、D为非金属元素,B与E同族,B与C同周期;②E的原子序数为奇数,A与E的原子序数之和为28;③0.1mol C单质与足量的E的最高价氧化物对应水化物的溶液反应生成3.36 L(标准状况)的氢气。请回答下列问题:
(1)C的单质与足量的E的最高价氧化物对应的水化物的溶液反应的离子方程式。
(2)B单质的最高价氧化物的水化物与D的最高价氧化物水化物之间相互反应生0.9 g水时,放出的热量为Q kJ,请写出该反应的热化学方程式。
(3)请用电子式表示D元素和E元素所构成的化合物的形成过程 。
。
(4)向⑴所得的溶液中通入过量的CO2气体,过滤后的滤液(不考虑过量二氧化碳的溶解)中各种粒子的数量的从大到小的排序为。
(5)C单质在日常生活和工业、农业、军事、科技等领域有广泛应用。如在海水中用碳棒和C单质做电极构成原电池,该原电池的正极的电极反应式为。