(本小题满分8分)某小河边有四座工厂:甲、乙、丙、丁(如图所示)。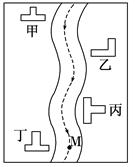
已知,它们所排出的废液里分别含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种。某环保小组对河水监测时发现:①甲处河水呈乳白色②乙处河水呈红褐色浑浊状③丙处河水由浑浊变清④丁处河水产生气泡,河水仍澄清。
请推断:
(1)四座工厂排出的废液里含有的污染物是甲 ,乙 ,丙 ,丁 。
(2)在M处取出的河水中,肯定大量存在的离子有 。
(3)用离子方程式表示丙除河水变澄清的原因: 。
烃A分子式为C4H10,分子结构中含有一个次甲基( ),则此物质A的二溴代物的种数为
),则此物质A的二溴代物的种数为
| A.3种 | B.4种 | C.5种 | D.以上都不对 |
在CO2中,Mg燃烧生成MgO和C。下列说法正确的是
A.元素C的单质只存在金刚石和石墨两种同素异形体
B.Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg)
C.在该反应条件下,Mg的还原性强于C的还原性
D.该反应中化学能全部转化为热能
下列关于物质或离子检验的叙述正确的是
| A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ |
| B.气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气 |
| C.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+ |
| D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2 |
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,蓝色溶液变为棕色。再向反应后的溶液中通入过量的SO2气体,溶液变成无色。则下列说法正确的是
| A.通入22.4 L SO2参加反应时,有2 NA个电子发生转移 |
| B.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
| C.滴加KI溶液时,KI被氧化,CuI是氧化产物 |
| D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。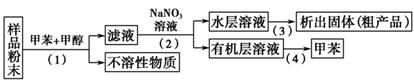
下列说法错误的是
| A.步骤(1)需要过滤装置 |
| B.步骤(2)需要用到分液漏斗 |
| C.步骤(3)需要用到坩埚 |
| D.步骤(4)需要蒸馏装置 |