对于温度与反应方向的关系,下列判断正确的是
| A.ΔH<0,ΔS>0,所有温度下反应都自发进行 |
| B.ΔH>0,ΔS>0,所有温度下反应都自发进行 |
| C.ΔH<0,ΔS<0,高温下反应自发进行 |
| D.ΔH>0,ΔS<0,所有温度下反应都自发进行 |
下列鉴别方法可行的是( )
| A.用氨水鉴别Al3+、Mg2+和Ag+ |
| B.用Ba(NO3)2溶液鉴别Cl-、SO42-和CO32- |
| C.菠菜中铁元素含量较高,为证明菠菜中的铁元素是+2价还是+3价,可把菠菜捣碎加水溶解,再向过滤后的滤液中加硫氰化钾溶液 |
| D.加入稀盐酸产生使澄清石灰水变浑浊的气体,则原溶液中一定含有CO32- |
用下面的方案进行某些离子的检验,其中方案设计严密的是( )
A.检验试液中的SO42-:试液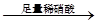 无沉淀 无沉淀 白色沉淀 白色沉淀 |
B.检验试液中的SO32-:试液 气体 气体 褪色 褪色 |
C.检验试液中的I-:试液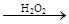 棕黄色溶液 棕黄色溶液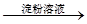 蓝色溶液 蓝色溶液 |
D.检验试液中的CO32-:试液 白色沉淀 白色沉淀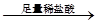 沉淀溶解 沉淀溶解 |
下列除去杂质的方法正确的是( )
| 物质(杂质) |
除杂方法 |
|
| A |
Cl2(HCl) |
将气体通过盛有氢氧化钠溶液的洗气瓶 |
| B |
CO2(HCl) |
将气体通过盛有饱和Na2CO3溶液的洗气瓶 |
| C |
氢氧化铁胶体 (FeCl3) |
将混合物直接过滤 |
| D |
SiO2 (CaCO3) |
加入盐酸后过滤 |
下列物质的检验,其结论一定正确的是( )
| A.某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,沉淀不溶解,则该溶液中一定含有SO42- |
| B.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中至少有SO32-和CO32-中的一种 |
| C.取少量Na2SO3样品于试管中加水溶解后加入盐酸有气体产生,再加入BaCl2溶液有白色沉淀产生,说明Na2SO3样品已部分被氧化 |
| D.能使湿润的淀粉碘化钾试纸变蓝的一定是Cl2 |
关于下列各装置图的叙述中,错误的是( )
| A.装置①用来电解饱和食盐水,c电极产生的气体能使湿润的淀粉KI试纸变蓝 |
| B.装置②可用于收集H2、NH3、Cl2、HCl、NO2 |
| C.装置③中X为苯,可用于吸收氨气或氯气 |
| D.装置④可用于干燥、收集氨气,并吸收多余的氨气 |