已知五种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径 |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+6,-2 |
+2 |
-2 |
下列叙述正确的是
A、L与T形成的化合物属于共价化合物 B、L、M的单质与稀盐酸反应速率:M>L
C、T、Q的氢化物常温常压下均为无色气体 D、M最高价氧化物的水化物具有两性
0.1 溶液的 最接近于
| A. | 5.6 | B. | 7.0 | C. | 8.4 | D. | 13.0 |
题文已知:
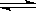 。该反应的达到平衡后,下列条件有利于反应向正方向进行的是
。该反应的达到平衡后,下列条件有利于反应向正方向进行的是
| A. | 升高温度和减小压强 | B. | 降低温度和减小压强 |
| C. | 降低温度和增大压强 | D. | 升高温度和增大压强 |
铁粉与含有 的 溶液完全反应后,得到 铜,则参与反应的 与 的物质的量之比为
| A. | 1∶7 | B. | 7∶1 |
| C. | 7∶8 | D. | 8∶7 |
下列反应的离子方程式正确的是
| A. | 锌片插入硝酸银溶液中: |
| B. | 碳酸氢钙溶液加到醋酸中: ↑ |
| C. | 少量金属钠加到冷水中: ↑ |
| D. | 氢氧化铜加到盐酸中: |
若 表示阿伏加德罗常数,下列说法正确的是()
| A. | 作为氧化剂得到的电子数为 |
| B. | 在 ,101 kPa时,22.4 L氢气中含有 个氢原子 |
| C. | 14 g氮气中含有7 个电子 |
| D. | 个一氧化碳分子和0.5 mol甲烷的质量比为7∶4 |