下列图示的四种实验操作名称从左到右依次是
| A.过滤、蒸发、蒸馏、分液 | B.过滤、蒸馏、蒸发、分液 |
| C.蒸发、蒸馏、过滤、分液 | D.分液、蒸馏、蒸发、过滤 |
能使KMnO4溶液褪色的是()
| A.苯 | B.乙烯 | C.乙醇 | D.乙酸 |
下列关于乙烯的叙述不正确的是()
| A.乙烯是组成最简单的烯烃; |
| B.乙烯是无色难溶于水的气体; |
| C.乙烯能发生取代反应、加成反应、但不能发生氧化反应; |
| D.乙烯可发生氧化反应,但只能被酸性KMnO4溶液氧化。 |
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结构如下图,下列关于该物质的说法正确的是( )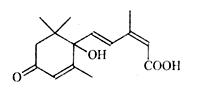

A.含有碳碳双键、羟基、羰基、羧基 |
B.含有苯环、羟基、羰基、羧基 |
C.含有羟基、羰基、羧基、酯基 |
D.含有碳碳双键、苯环、羟基、羰基 |
每年的6月26日是国际禁毒日,珍爱生命,远离毒品。以下是四种毒品的结构简式,下列有关说法正确的是( )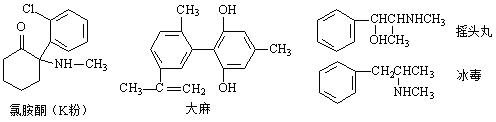
| A.四种毒品都属于芳香族化合物,都难溶于水 82615205 |
B.摇头丸和冰毒互为同分异构体 |
C.1mol大麻与溴水反应最多消耗4mol Br2 |
| D.大麻分子中所有碳原子不可能共平面 |
以下各组物质可以用分液漏斗分离的是 ( )
| A.硝基苯和水 | B.乙醇和水 |
| C.甲醛和水 | D.乙酸乙酯和乙酸 |