CuSO4溶液是中学化学及工农业生产中常见的一种试剂。
(1)配制CuSO4溶液时,需加入一定量的硫酸溶液,用离子方程式说明其原因是 。
(2)利用配制的CuSO4溶液及如图所示装置,进行以下实验探究。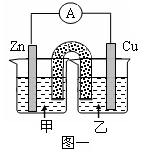
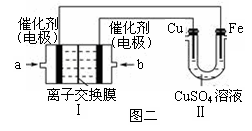
①图一是根据反应Zn+CuSO4 Cu+ZnSO4设计成的锌铜原电池。甲池中的电解质溶液为 (填化学式)______________,Cu极的电极反应式是__________________,盐桥中是含有琼胶的KCl饱和溶液,电 池工作时Cl-向________(填“甲”或“乙”)池移动。
②图二中,Ⅰ是氢气燃料电池(电解质溶液为KOH溶液)的结构示意图,电池总反应为:2H2+O2=2H2O。该同学想在Ⅱ中实现铁上镀铜,则a处加入的是________(填“H2”或“O2”),b处电极上发生的电极反应式是_____________________。
③若把图二Ⅱ中电极均换为惰性电极且CuSO4溶液足量,电解时的化学反应方程式为 ,
一段时间后,反应停止。下列物质能使Ⅱ池恢复到反应前浓度的是________(填选项字母)。
| A.Cu | B.CuO | C.CuCO3 | D.Cu(OH)2 |
(15分)化学——选修3:物质结构与性质
Ⅰ.已知砷化镓的晶胞结构如图所示。请回答下列问题:
(1)下列说法正确的是__________(填序号)
| A.砷化镓晶胞结构与NaCl相同 | B.第一电离能 As>Ga |
| C.电负性 As>Ga | D.原子半径 As>Ga |
(2)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的方程式为:__________________________
(3)AsH3空间形状为___________;已知(CH3)3Ga为非极性分子,则其中镓原子的杂化方式为____________;
Ⅱ.金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(4)请解释金属铜能导电的原因 ,Cu2+的核外电子排布式为________________。
(5)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3) 4]SO4晶体,晶体中含有的化学键除普通共价键外,还有和。
选考(15)化学与技术
侯氏制碱法的生产流程可表示如下,请回答下列问题: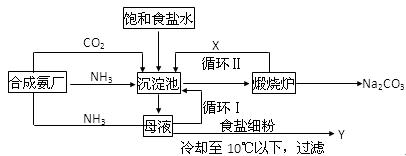
(1)沉淀池中加入(或通入)有关物质的顺序为_____________→___________→___________
(2)写出上述流程中X、Y的化学式:X____________Y___________
(3)写出沉淀池中发生的化学反应方程式__________________________________________
(4)侯氏制碱法的生产流程中可以循环使用的物质主要为____________、______________
(5)从沉淀池中取出沉淀的操作是___________,为了进一步提纯NaHCO3晶体,可采用_______法
(6)若在煅烧炉中燃烧的时间较短,NaHCO3将化解不完全。现若取10.5g NaHCO3固体,加热一定时间后,剩余固体的质量为7.1g,如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,充分反应后溶液中H+的物质的量浓度为___________mol/L(溶液体积变化忽略不计)
CO是水煤气的主要成份之一,是一种无色剧毒气体,根据信息完成下列各题
Ⅰ、已知下列热化学方程式
2C(s) + O2(g) = 2CO(g) △H = -221kJ/mol
C(s) + O2(g) = CO2(g) △H = -393kJ/mol
24g单质碳在不足量的O2中燃烧时,生成等物质的量的CO和CO2气体,则和24g单质碳完全燃烧生成CO2相比较,损失热量_________kJ
Ⅱ、850℃时,在10L体积不变的容器中投入2molCO和3molH2O,发生如下反应:
CO(g) + H2O(g)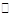 CO2(g) + H2(g)
CO2(g) + H2(g)
当CO的转化率达60%时,反应达平衡
(1)850℃时,该反应的平衡常数为_________
(2)该条件下,将CO和H2O都改为投入2mol,达平衡时,H2的浓度为_________mol/L,下列情况能说明该反应一定达平衡的是_________
| A.CO和H2O蒸气的浓度之比不再随时间改变 |
| B.气体的密度不再随时间改变 |
| C.CO和CO2的浓度之比不再随时间改变 |
| D.气体的平均摩尔质量不再随时间改变 |
Ⅲ、为防止CO使人中毒,一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇——氧化钠,其中O2-可以在固体NASICON中自由移动,则:
(1)该原电池中通入CO的电极为_________极,该电极的电极反应式为___________________
(2)通空气一极的电极反应式为____________________________________
(15分)某工业废液中含有Cu2+、Mg2+、Zn2+等离子,为将其回收利用,再采用了如下工艺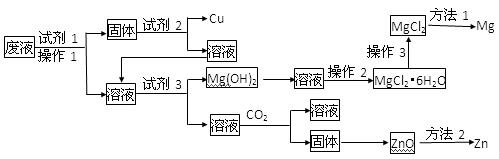
已知Zn(OH)2的性质与Al(OH)3相似
所用试剂在下列试剂中选择
① 铁粉 ②锌粉 ③稀HNO3 ④稀H2SO4 ⑤稀HCl ⑥稀氨水 ⑦NaOH溶液 ⑧石灰水
请回答下列问题:
(1)试剂1、试剂2、试剂3分别可以是________、________、________(填编号)
(2)操作2是__________________、_____________________、___________________
(3)操作3是__________________________________________________________
(4)加过量CO2时发生反应的离子方程式___________________________________
(5)在金属冶炼方法中方法1是_________方法2是____________
氮化铝(AlN)广泛应用于集成电路,其制备原理是将氧化铝与碳粉混合均匀,在持续流动的氮气流中加热至1750℃,发生如下反应:
(1)断开N2分子内的共价键要热量(填“吸收”或“放出”)
(2)分析反应②对①、③平衡移动的影响。
(3)Al2O3、C、N2合成AlN的平衡常数表达式K=。
(4)用蒸馏法测定产品中AlN的含量,装置如下(加热及夹持装置略):
①AlN与NaOH溶液反应产生NH3的化学方程式是。
②锥形瓶内吸收NH3的离子方程式是。
③检验NH3是否完全蒸出的方法是:另取少量蒸馏出的溶液,(将检验过程补充完整)。
④NH3完全吸收后,向锥形瓶中加入指示剂,用浓度为c((N aOH)mol/L的NaOH标准溶液滴定过量的H2SO4,终点时用去标准溶液的体积为 。下面有关计算正确的是。
。下面有关计算正确的是。
A.样品中AlN的质量:
B.AlN的质量分数:
C.锥形瓶吸收NH3的物质的量: