反应A+B →C分两步进 行:①A+B→X,②X →C,反应过程中能量变化如图所示,E1表示反应A+ B→X的活化能。下列有关叙述正确的是
| A.E2表示反应X→C的活化能 |
| B.X是反应A十B→C的催化剂 |
| C.反应A十B→C的△H<0 |
| D.加入催化剂可改变反应A十B→C的焓变 |
已知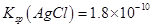 ,
, 。下列关于不溶物之间转化的说法中错误的是:
。下列关于不溶物之间转化的说法中错误的是:
A. 不溶于水,不能转化为 不溶于水,不能转化为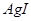 |
B.两种不溶物的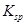 相差越大,不溶物就越容易转化为更难溶的不溶物 相差越大,不溶物就越容易转化为更难溶的不溶物 |
C.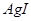 比 比 更难溶于水,所以, 更难溶于水,所以, 可以转化为 可以转化为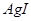 |
D.常温下, 若要在 若要在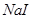 溶液中开始转化为 溶液中开始转化为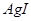 ,则 ,则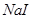 的浓度必须不低于 的浓度必须不低于 |
下列图示与对应的叙述相符的是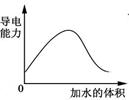

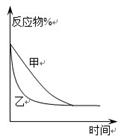
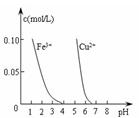
图Ⅰ图Ⅱ图Ⅲ图Ⅳ
| A.图Ⅰ表示t℃时冰醋酸在稀释过程中溶液导电性的变化 |
| B.图Ⅱ表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
C.图Ⅲ表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的大 3C(g)+D(s)的影响,乙的压强比甲的大 |
| D.据图Ⅳ,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右 |
物质的量浓度相同的NaOH和HCl溶液以3∶2体积比相混合,所得溶液的pH=12。则原溶液的物质的量浓度为
| A.0.01 mol·L-1 | B.0.017 mol·L-1 | C.0.05 mol·L-1 | D.0.50 mol·L-1 |
一定温度下,在固定容积、体积为2 L的密闭容器中充入1 mol N2和3 mol H2发生反应,当反应进行到10 s末时反应达到平衡,此时容器中c(NH3)=0.1mol·L-1。下列有关判断错误的是
| A.反应达平衡时N2的转化率为10% |
| B.反应进行到10 s末时,H2的平均反应速率是0.03 mol·(L·s)-1 |
| C.该反应达到平衡时,N2的平衡浓度为0.45 mol/L |
| D.该反应达到平衡时的压强是起始时压强的0.95倍 |
下列说法中正确的是
| A.将纯水加热至较高温度,Kw变大、pH变小、呈酸性 |
| B.保存FeSO4溶液时,应在其中加入稀HNO3以抑制Fe2+水解 |
| C.AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 |
D.向0.1 mol·L-1氨水中加入少量水,pH减小,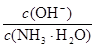 增大 增大 |