氢气是一种理想的“绿色能源”,下图为氢能产生与利用的途径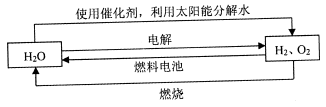
(1)上图中4个过程中能量转化形式有_____________
| A.2种 | B.3种 | C.4种 | D.4种以上 |
(2)电解过程要消耗大量电能,而使用微生物作催化剂在阳光下即可分解
2H2O(1) 2H2(g)+O2(g)△H1
2H2(g)+O2(g)△H1
2H2O(1) 2H2(g)+O2(g)△H2
2H2(g)+O2(g)△H2
以上反应的△H1_____________△H2 (选填“>"、“<”或“=”)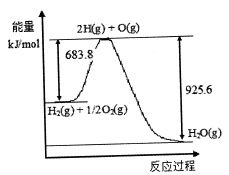
(3)已知H2 O(1)→H2 O(g)△H=" +44" mol·L-1,依据右图能量变化写出氢气燃烧生成液态水的热化学方程式________________________________。
(4)氢能利用需要选择合适的储氢材料
①镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g) LaNi5H6(s) △H<0,欲使LaNi5H6 (s)释放出气态氢,根据平衡移动原理,可改变的条件之一是__________________。
LaNi5H6(s) △H<0,欲使LaNi5H6 (s)释放出气态氢,根据平衡移动原理,可改变的条件之一是__________________。
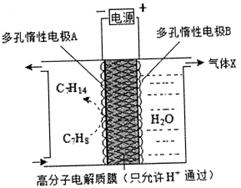
②一定条件下,如图所示装置可实现有机物的电化学储氢,总反应:2C7 H8+6 H2O(1) 2C7 H14+3O2 (g),电解过程中产生的气体X为_____,电极A发生的电极反应式为_________________。
2C7 H14+3O2 (g),电解过程中产生的气体X为_____,电极A发生的电极反应式为_________________。
ClO2气体是一种常用的消毒剂,近几年我国用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,由此说明ClO2具有___________性。
(2)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式:2KClO3+SO2==="=" 2ClO2+____________。
(3)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O+I2===S4O+2I-)
Ⅲ.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如图所示:
请回答:
①操作Ⅰ中反应的离子方程式是__________________。
②确定操作Ⅱ完全反应的现象是___________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是_______________________。
④若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是__________mg·L-1。
减少二氧化碳的排放以及资源化利用具有重要意义。
(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式如下:6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △H=-76.0 kJ·mol一1,
C(s) +2H2O(g) = CO2(g) + 2H2(g) △H="+113.4" kJ·mol一1;
则反应:3FeO(s)+ H2O(g)= Fe3O4(s)+ H2(g)的△H=__________。
(2)目前 (NH4)2CO3已经被用作工业捕碳剂,为研究温度对(NH4)2CO3捕获CO2效率的影响,在T1温度下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,得到趋势图(见图2)。则:
①该反应的ΔH 0(填“>”、“=”或“<”)。
②在T1~T2及T4~T5两个温度区间,容器内CO2气体浓度呈现如图2所示的变化趋势,其原因是 。
③该反应在温度为T1时,溶液pH随时间变化的趋势曲线如图1所示。当时间到达t1时,将该反应体系温度迅速上升到T2,并维持该温度。请在该图中画出t1时刻后溶液的pH变化总趋势曲线。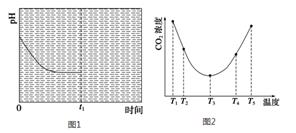
(3)利用该反应捕获CO2,在(NH4)2CO3初始浓度和体积确定的情况下,提高CO2吸收量的措施有 (写出两条)。
氮及其化合物在生产、生活中有着重要作用,减少氮氧化物的排放是环境保护的重要内容之一,请回答下列氮及其化合物的相关问题:
(1)N4的分子结构与白磷分子的正四面体结构相似。已知断裂1mol N-N键吸收167kJ热量,生成1mol N≡N键放出942kJ热量,请写出N4气体转变为N2反应的热化学方程式: 。
(2)NH3可直接用作车用燃料电池,产物无污染。写出碱性介质下该电池负极的电极反应式: 。
(3)在T1℃时,将5mol N2O5置于10L固定容积的密闭容器中发生下列反应:2N2O5(g)  4NO2(g)+O2(g);△H>0;反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%。
4NO2(g)+O2(g);△H>0;反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%。
①T1℃时该反应的平衡常数K的计算式为 。
②用O2表示从0~5min内该反应的平均速率υ(O2) = 。
③将上述平衡体系的温度降至T2℃,密闭容器内减小的物理量有 。
A.压强 B.密度 C.反应速率 D.N2O5的浓度
(4)在恒温恒容的密闭容器中充入NO2,建立如下平衡:2NO2(g)  N2O4(g),平衡时N2O4与NO2的物质的量之比为a,其它条件不变的情况下,分别再充入NO2和再充入N2O4,平衡后引起的变化正确的是 。
N2O4(g),平衡时N2O4与NO2的物质的量之比为a,其它条件不变的情况下,分别再充入NO2和再充入N2O4,平衡后引起的变化正确的是 。
A.都引起a减小
B.都引起a增大
C.充入NO2引起a减小,充入N2O4引起a增大
D.充入NO2引起a增大,充入N2O4引起a减小
(5)25℃时,NH3·H2O电离常数Kb=1.8×10-5,Mg(OH)2的溶度积常数Ksp=1.8×10-11,用pH计测得0.5 mol·L一1氨水溶液的pH约为 。在某氯化镁溶液中加入一定量某浓度的氨水后,测得混合液pH =11.0,则此温度下残留在溶液中的c(Mg2+)= 。(已知lg2≈0.3、lg3≈0.5)。
NH4NO3主要用作肥料、军用炸药、冷冻剂、制造笑气等。
(1)铵态氮肥NH4NO3________(填“能”或“不能”)与草木灰混合施用,用盐类水解的知识简述原因__________。
(2)NH4NO3受热分解温度不同,分解产物也不同。在185~200°C时,NH4NO3分解生成笑气(N2O)和水,分解生成的氧化产物与还原产物的质量比为__________。超过400°C,NH4NO3剧烈分解生成N2、NO2和H2O,并发生爆炸,若32g NH4NO3爆炸放出12.3 kJ的热量,则NH4NO3分解爆炸的热化学方程式为______________。
(3)电解NO制备 NH4NO3,其工作原理如图所示,阴极反应式为___________________;电解反应的总方程式为___________________;为使电解产物全部转化为NH4NO3,需补充物质A,A是__________。
NaCN、KCN等氰化物是重要的基本化工原料。用于基本化学合成、冶金等。
(1)用含NaCN(N显一3价)的废水合成黄血盐(K4[Fe(CN)6])的主要工艺流程如图:
①写出NaCN的电子式__________。
②在反应器中发生的主要反应的方程式为 。
③加入碳酸钠溶液主要目的是 。
(2)已知HCN的电离常数Ka=6.2×10-10,浓度均为0.1mol·L-1的NaCN和HCN的混合溶液显 (填“酸”、“碱”或“中”) 性,通过计算说明原因 。
(3)现代开采金矿:先以NaCN溶液浸取粉碎的含金(Au)矿石,通空气,使矿石中的金粒溶解,得到Na[Au(CN)2]( 二氰合金酸钠)溶液;再用锌与Na[Au(CN)2]溶液发生置换反应生成金。金溶解过程中发生的化学方程式为 ;消耗的锌与生成的金的物质的量之比为 。
(4)臭氧(O3)可以将剧毒的NaCN溶液氧化为无毒的NaCNO, 进一步将NaCNO氧化得到N2和NaHCO3,在氧化过程中,1mol O3得到2mole-。若要处理含NaCN0.001mol·L-1103L,至少需要标准状况下的O3 L。