油脂是高级脂肪酸的甘油酯,在工业上用途广泛。
实验一:用地沟油制肥皂(高级脂肪酸钠盐)和甘油(常压下甘油的沸点为290℃)。
32将约6g地沟油、10mL 40%的烧碱溶液、5mL液体A混合后在烧杯中加热约0.5小时。A可以增大反应物间的接触,则A可以是 _____(选填编号)。
a.四氯化碳 b.汽油 c.乙醇
33.从皂化反应后的溶液中提取肥皂和甘油的过程如下:
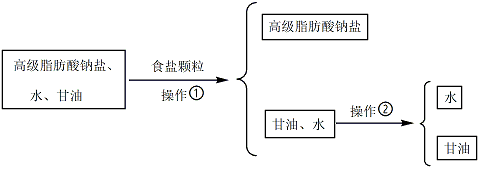
加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是 。操作②必须用到的玻璃仪器是_____(选填编号)。
a.漏斗 b.分液漏斗 c.蒸馏烧瓶
34.若甘油的产率明显低于高级脂肪酸钠盐的产率,可能的原因是_____(选填编号)。
a.油脂水解不充分 b.部分甘油挥发 c.甘油中混有水
实验二:测定油脂的碘值。碘值是指100g油脂中所能吸收(加成)碘的克数。
称取a g某油脂,加入含bmol I2的溶液(韦氏液),充分振荡;过量的I2用cmol/L Na2S2O3溶液滴定(以淀粉为指示剂):2Na2S2O3+ I2 =Na2S4O6+ 2NaI用去vmL。
35.配制韦氏液,溶剂选用冰醋酸而不选用水的原因是 。
滴定终点时颜色的变化是 。
36.该油脂的碘值为(用相关字母表示) 。
37.冰醋酸也会消耗Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值偏_____(选填“高”或“低”)。
A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
| 阳离子 |
Na+、Al3+、Ba2+、NH4+ |
| 阴离子 |
Cl-、OH-、CO32-、SO42- |
分别取四种物质进行实验,实验结果如下:
①A、D溶液呈碱性,B呈酸性,C呈中性
②A溶液与B溶液反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失
③A溶液与D溶液混合并加热有气体生成,该气体能使湿润的红色石蕊试纸变蓝
回答下列问题:
(1)A的化学式是_________,用电子式表示C的形成过程:________________ 。
(2)向A溶液中通入适量CO2,使生成的沉淀恰好溶解,所得溶液中各离子物质的量浓度由大到小的顺序是:________________________ 。
(3)写出③的离子方程式_______________________________________________ 。
(4)简述D溶液呈碱性的理由___________________________________________ 。
Heck反应是合成C—C键的有效方法之一,如反应①:
化合物Ⅱ可由以下合成路线获得:
Ⅳ(分子式C3H6O3) Ⅴ
Ⅴ Ⅱ
Ⅱ
(1) 化合物Ⅲ的分子式为__________,1 mol化合物Ⅲ最多可与__________mol H2发生加成反应。
(2)化合物Ⅳ分子结构中有甲基,写出由化合物Ⅳ反应生成化合物Ⅴ的化学方程式
________________________________________________________________________
________________________________________________________________________。
(3)有关化合物Ⅱ说法正确的是( )
| A.1 mol 化合物Ⅱ完全燃烧消耗5 mol O2 |
| B.化合物Ⅱ能使酸性高锰酸钾溶液褪色 |
| C.化合物Ⅱ难溶于水 |
D.化合物Ⅱ分子间聚合,反应生成的高聚物结构为 |
(4)化合物Ⅲ的一种同分异构体Ⅵ,苯环上的一氯取代物有两种,Ⅵ能与NaHCO3溶液反应生成无色气体,除苯环上的氢外核磁共振氢谱还有四组峰,峰面积之比为1∶1∶1∶3,Ⅵ的结构简式为________________________________________________________________________。
(5)CH3Ⅰ和O也可以发生类似反应①的反应,有机产物的结构简式为__________________________________。
已知α氨基酸与亚硝酸(HNO2)反应生成α羟基酸。如: 试根据下列6种有机物之间的转化关系,回答有关问题:
试根据下列6种有机物之间的转化关系,回答有关问题:
(1)写出有机物B和E的结构简式。
B:____________________,E:____________________。
(2)写出下列反应的化学方程式。
①A→C:________________________________________________________________________。
②D→F:________________________________________________________________________。
醛可以跟亚硫酸氢钠的饱和溶液发生加成反应,生成物是水溶性的α羟基磺酸钠: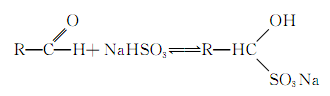
反应是可逆的,在通常条件下有70%~90%向正反应方向转化。
(1)若溴苯中混有杂质苯甲醛,欲将此杂质全部除去,可采用的试剂是__________________,其分离方法为__________________。
(2)若在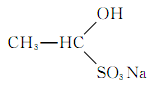 水溶液中加入足量盐酸,有机物转化为________,将该转化产物分离出来的常用方法是________。
水溶液中加入足量盐酸,有机物转化为________,将该转化产物分离出来的常用方法是________。
X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。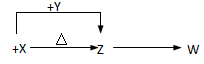
(1)W的电子式是____________ 。
(2)X与Y在溶液中反应的离子方程式是_______________ 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置V中可收集到一种无色气体。
①装置I中反应的化学方程式是_________ , 装置II中物质的化学式是 ____________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置V中气体,该化合物的化学式是________ ,所需仪器装置是_________ (从上图选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是 ______________。