物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)将10.6 g Na2CO3溶于水配成1 L溶液
①该溶液中Na2CO3的物质的量浓度为_______,溶液中Na+的物质的量浓度为________。
②向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4 mol·L-1(假设溶液体积不变)需加入NaCl的质量为_____,Cl-的物质的量浓度为_____ 。
(2)把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为 。
(3)在P+CuSO4+H2O―→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为_______mol。生成1 mol Cu3P时,参加反应的P的物质的量为_______mol。
某元素的最高价氧化物的水化物的分子式为HxROy,气态氢化物的化学式为HzR。已知1 mol HxROy比1molHzR质量多64g,又知1molHxROy中R的核外电子总数比1molHxROy中氢原子和氧原子核外电子总数少16mol,试求R的原子序数。
某原子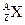 的氯化物XCl2 1.11g配成溶液后,需用1mol·L-1的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的氯化物XCl2 1.11g配成溶液后,需用1mol·L-1的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
(1)X的质量数。
(2)若X的核内中子数为20,求22.2gXCl2中所含质子的物质的量是多少?
今有CH4、HCHO、O2三种成分的混合气体,同温同压下与乙烷气体的密度相同。问:
(1)混合气体中CH4和O2的物质的量之比为多少?
(2)若某条件下水为气态,气体的摩尔体积为50 L·mol-1,在该条件下点燃混合气体,混合气恰好完全燃烧,共生成CO2 13.2 g,求原混合气体中氧气的物质的量和生成的混合气体在该条件下的密度。
(经典回放)
阅读下列短文,完成问题:
汽车作为曾经推动人类文明向前跃进的现代社会的产物,在给人类的生活带来便捷舒适的同时,对自然生态环境的恶化也有难以推卸的责任。据6月15日我市政府发布的“2000年厦门环境状况公报”称:厦门大气污染主要来源于工业污染和汽车尾气,99%的一氧化碳和一氧化氮的排放来源于汽车尾气。我市近几年来汽车持有量的增长达20%,虽然空气质量居全国第四,但环保仍面临如汽车污染等问题的考验。
另据报道:将氢气应用于汽车发动机的技术已在我国研制成功;酒精作为燃料的汽车已在北京市、河南省使用;我市也有一部分汽车改用液化气作为燃料。
(1)汽车尾气中的大气污染物有(写化学式)____________,____________。
(2)我市将部分汽车排气管加装三效转换器,促使一氧化碳在排气管内与空气作用转化为二氧化碳,其反应式为
____________________________________________________________。
(3)请提出我市治理汽车污染的一条合理化建议:
____________________________________。
(4)就目前的情况看,氢气做燃料的汽车要投入使用前,你认为还要研究解决的问题有:_____________________________________________________________________________。
(5)若实验用氢气汽车运行1 km,需要2 858 kJ能量。现这辆汽车在我市环岛路上走一圈(约30 km),需要____________g氢气。(已知每克氢气燃烧放出142.9 kJ能量。)
利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如下图所示的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。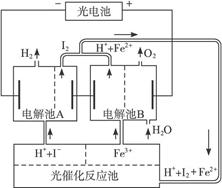
(1)写出电解池A、电解池B和光催化反应池中反应的离子方程式。
(2)若电解池A中生成3.36 L H2(标准状况),试计算电解池B中生成Fe2+的物质的量。
(3)若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为a mol·L-1和b mol·L-1,光催化反应生成Fe3+的速率为c mol·L-1,循环系统中溶液的流量为Q(流量为单位时间内流过的溶液体积)。试用含所给字母的代数式表示溶液的流量Q。