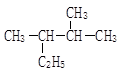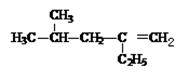(1)材料是人类赖以生存和发展的重要物质基础。
①生产水泥的主要原料是黏土和 (填名称)。
②橡胶是制造轮胎的重要原料,天然橡胶通过硫化措施可增大强度和弹性,硫化后的橡胶是 结构。(选填“线型”或“体型”)。
(2)人体健康与食品关系密切。
①有些学生从小偏食,不爱吃水果、蔬菜,结果营养缺乏、发育不良,这主要是由于摄取 (选填“脂肪”、“维生素”或“蛋白质”)不足引起的。
②生活中应合理地摄取人体必需的元素,体内 元素含量过低,会引起甲状腺疾病。
③糖类、油脂、蛋白质都是人体必需的营养物质。其中蛋白质被摄入人体后,在酶的作用下水解为 (写名称)。
(3)人体健康与药物等关系密切:
人的纯净胃液是一种无色液体,呈酸性,PH在0.9~1.5之间,其中H+的浓度比血液中高几万倍,回答下列问题:
①液有帮助人体消化食物等多种功能,胃酸的主要成份是
②若胃酸酸度增大就会患胃酸过多症,下列物质不宜用做治疗胃酸过多的药物是
| A.小苏打 | B.氢氧化铝 | C.氢氧化钠 | D.碳酸镁 |
③胃舒平的主要成份是氢氧化铝,不溶于水且作用持久,写出该药物中和胃酸的离子方程式 。
④可以帮助流感病人解热镇痛的药物是 (选填“青霉素”或“阿司匹林”)。
(4)洁净安全的生存环境更是健康的保障。
①某农村地区洪涝灾害后为获得饮用水,在将地表水取回家后,先加明矾,再过滤,去除悬浮在水中的较大颗粒;过滤后常使用漂白粉进行杀菌消毒,
其原理可用化学方程式表示为 。
②氯气与氢氧化钙溶液反应能制得漂白粉。试写出工业制漂白粉反应的化学方程式: 。
③通道口设有专门垃圾箱,箱体上标有下图所示,下图图标表示 。
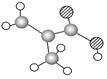
A B C
(1)图A是由4个碳原子结合成的某种烷烃(氢原子没有画出)。
①写出该有机物的系统命名法的名称。②该有机物的同分异构体的核磁共振氢谱中应有个峰
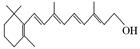
(2)图B的键线式表示维生素A的分子结构。
①该分子的化学式为。②1 mol维生素A最多可与mol H2发生加成反应。
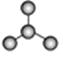
(3)某物质只含C、H、O三种元素,其分子模型如图C所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
①该物质的结构简式为
②该物质中所含官能团的名称为和
从以下6种物质中选取序号填空(仅填序号,可重复选填)。
①二氧化碳;②硫化氢;③氯化铵;④氢氧化钾;⑤乙炔;⑥乙醇
(1)含有非极性键的是;
(2)既含有σ键又含有π键的是;
(3)含有配位键的是;
(4)分子的立体结构呈V形的是;
(5)属于非极性分子的是;
(6)属于离子化合物的是。
已知:CH3—CH=CH2+HBr→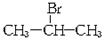 (主要产物),1 mol某芳香烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下面所示的一系列变化。
(主要产物),1 mol某芳香烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下面所示的一系列变化。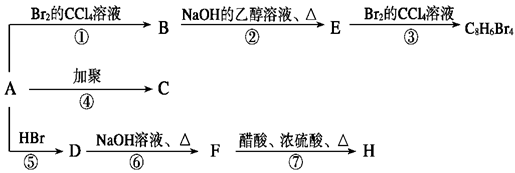
(1)A的结构简式:。
(2)上述反应中,①是反应,⑦是反应。(填反应类型)
(3)写出C,E物质的结构简式:C, E,
(4)写出D→F反应的化学方程式。
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为;
(2)A中的碳原子是否都处于同一平面?(填“是”或“不是”);
(3)已知A、B、C有如下转化关系: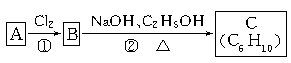
则反应②的化学方程式为;C的化学名称是。
(1)下列各化合物中,属于同系物的是,
属于同分异构体的是 填入编号)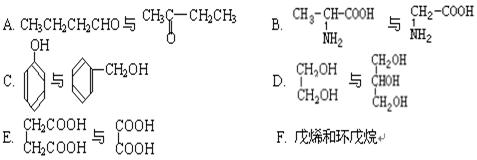
(2)系统命名法命名下列物质