在乙烯分子中有5个σ键和一个π键,它们分别是
| A.sp2杂化轨道形成σ键,未杂化的2p轨道形成π键 |
| B.sp2杂化轨道形成π键,未杂化的2p轨道形成σ键 |
| C.C—H之间是sp2杂化轨道形成σ键,C—C之间只有未杂化的2p轨道形成π键 |
| D.C—C之间是sp2杂化轨道形成σ键,C—H之间是未杂化的2p轨道形成π键 |
某同学为完成反应:2HCl+2Ag=2AgCl↓+H2↑设计了下列四个实验,如图所示,你认为可行的是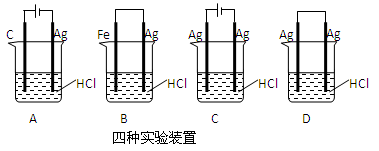
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:
FePO4+Li LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和锂,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨和锂,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是
A.可加入硫酸溶液以提高电解质的导电性 B放电时电池内部Li+向负极移动
C.充电过程中,电池正极材料的质量增加 D.放电时电池正极反应为:FePO4+e-+Li+=LiFePO4
2013年,科学家们发明了一种能够给电子设备提供动力的生物电池。该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的槽中。由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示。下列说法正确的是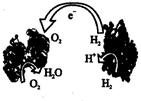
| A.左边为该电池的负极 | B.该电池可在高温环境下使用 |
| C.该电池负极反应为:H2-2e-==2H+ | D.该电池正极反应为:O2+4e-==2O2- |
下列过程或现象与盐类水解无关的是
| A.用热的纯碱溶液去油污 | B.铁在潮湿的环境下生锈 |
| C.加热氯化铁溶液颜色变深 | D.浓硫化钠溶液有臭味 |
往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。则原溶液中c(I-)/c(Cl-)的比值为
| A.(V2-V1)/V1 | B.V1/V2 | C.V1/(V2-V1) | D.V2/V1 |