17、下列反应的离子方程式书写正确的是
| A.硫酸镁固体加入氢氧化钠溶液: MgSO4+2OH-= Mg(OH)2↓+SO42- |
| B.碳酸钙溶于盐酸:CO32—+ 2H+ = CO2↑ + H2O |
| C.铜跟稀硝酸反应:3Cu+ 8H++2NO=3Cu2++2NO↑+4H2O |
| D.铁和稀硝酸反应:Fe+2H+=Fe2++H2↑ |
以下有关原子结构及元素周期律的叙述正确的是( )
| A.第IA族元素铯的两种同位素137Cs比133Cs多4个质子 |
| B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
| C.第ⅦA元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同主族元素从上到下,单质的熔点逐渐降低 |
下列物质中,既含离子键,又含共价键的是()
| A.NaCl | B.H2O | C.MgCl2 | D.NaOH |
下列关于价电子构型为3s23p4的粒子描述正确的是()
| A.它的元素符号为O |
| B.它的核外电子排布式为1s22s22p63s23p4 |
| C.它可与H2生成液态化合物 |
| D.其电子排布图为: |

1s 2s 2p 3s 3p
下列分子的电子式书写正确的是()
A.氨气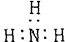 |
B.四氯化碳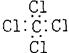 |
C.氮气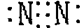 |
D.二氧化碳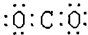 |
下列物质的分子中既有σ键,又有π键的是( )
①HCl ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥C2H2
| A.①②③ | B.③④⑤⑥ | C.③⑤⑥ | D.①③⑥ |