向含有下列离子的溶液中分别加入Na2O2(忽略溶液体积的变化),离子浓度基本不变的是
| A.AlO2- | B.Na+ | C.Fe2+ | D.HCO3- |
下列反应中,不需要使用催化剂的是
| A.乙烯和氢气反应 | B.乙烯和水反应 |
| C.乙炔和溴水反应 | D.乙炔和氯化氢反应 |
20世纪80年代后,人们发现和证实了碳的另一类单质,它们是由一系列偶数个碳原子组成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性。下图所示为n个C60连接而成的物质X。下列有关说法不正确的是
| A.X难溶于水 | B.X的摩尔质量为720n |
| C.X是碳的一种同素异形体 | D.一定条件下X可与H2发生加成反应 |
下列物质属于纯净物的是
| A.甲烷与氯气在光照下取代的有机产物 | B.液化石油气 | C.氯仿 | D.汽油 |
为了减少城市空气污染,要求使用无铅汽油,所谓无铅汽油是指
| A.不用铅桶装的汽油 | B.不含四乙基铅的汽油 |
| C.不含硝酸铅的汽油 | D.不含氧化铅的汽油 |
以下方程式的书写不正确的是
A.卤代烃的水解: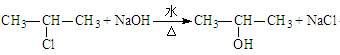 |
B.苯酚与碳酸钠溶液反应: |
| C.银氨溶液的配制总反应:Ag++ 2NH3·H2O = Ag(NH3)2++ 2H2O |
D.醇的消去: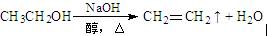 |