X、Y均为元素周期表ⅦA族中的两种元素。下列叙述中,能够说明X的原子得电子能力比Y强的是
| A.原子的电子层数:X>Y |
| B.对应的简单离子的还原性:X>Y |
| C.气态氢化物的稳定性:X>Y |
| D.氧化物对应水化物的酸性:X>Y |
等质量的铝粉与足量盐酸在不同条件下反应,产生H2的体积与反应时间关系如下图所示,则图中曲线a、b、c分别对应表中的实验组别是()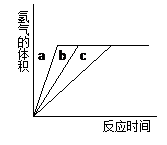
| 实验组别 |
盐酸浓度(mol/L) |
温度(℃) |
| ① |
2.00 |
15 |
| ② |
2.00 |
30 |
| ③ |
4.00 |
30 |
A.①—②—③ B.②—①—③ C.②—③—① D.③—②—①
根据下列实验方法和现象,得出结论正确的是()
A.某溶液 生成白色沉淀,则原溶液中一定含有Cl— 生成白色沉淀,则原溶液中一定含有Cl— |
B.某溶液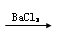 生成白色沉淀,则原溶液中一定含有SO42— 生成白色沉淀,则原溶液中一定含有SO42— |
C.某溶液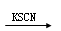 溶液呈红色,则原溶液中一定含有Fe3+ 溶液呈红色,则原溶液中一定含有Fe3+ |
D.某溶液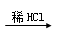 有气体产生,则原溶液中一定含有CO32— 有气体产生,则原溶液中一定含有CO32— |
根据右图装置判断下列说法错误的是()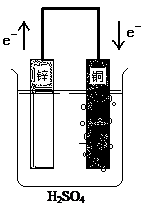
| A.铜片上有气泡产生 |
| B.铜片上发生氧化反应 |
| C.锌片为负极 |
| D.该装置将化学能转化为电能 |
下列离子或分子在溶液中能大量共存的一组是()
| A.Na+、OH—、Cl2 | B.Na+、Ca2+、CO32— |
| C.Na+、SO42—、NO3— | D.NH4+、NO3—、OH— |
下列叙述正确的是()
| A.H2O的摩尔质量为18g |
| B.16克CH4含有的分子数为6.02×1023 |
| C.常温、常压下1molNH3的体积约为22.4L |
| D.1L1mol·L—1Na2SO4溶液中含Na+为2mol |