下图是甲、乙两种固体物质的溶解度曲线。据图回答: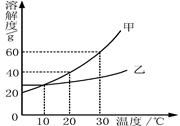
(1)10℃时,甲物质的溶解度 乙物质的溶解度(填“>”或“=”或“<”)。
(2)30℃时,等质量的甲、乙两饱和溶液降温到10℃, 析出晶体较多。
(3)20℃时,将50g甲物质放入盛有100g水的烧杯中,最终所得溶液的质量为 g;若将烧杯内物质升温到30℃(不考虑水蒸发),溶液中不变的是 (填序号)。
| A.溶剂的质量 | B.溶液的质量 |
| C.溶质的质量分数 | D.以上都不变 |
(4)30℃时,当甲的饱和溶液中含有少量乙时,若要提纯出较多的甲,应采取的方法是 。
西北区域气候中心对我省2013年3月气候影响做出评价,3月全省平均气温为近54年同期最高,降水为近51年同期最少.水是生命之源,持续的干旱,造成了人畜饮水困难,各地积极采取措施抗旱.请回答下列问题:
(1)保持水化学性质的微粒是(填名称);
(2)有些村民打井取用地下水,他们通常用的方法降低地下水的硬度;你能用测定水的酸碱度;向河水中加明矾和漂白粉净化后,河水可作为生活用水,其中明矾的作用是,漂白粉中的有效成分是次氯酸钙[
],次氯酸钙中氯元素的化合价是.
(3)为了缓解旱情,气象部门适时实施人工降雨.常用作人工降雨的物质是.
(4)"节约用水,从我做起"请你任举一例生活中节约用水的措施:.
写出下列化学符号的意义或题目所要求的化学符号.
(1)2
(2)2个氮分子
(3)
(4)五氧化二磷中磷元素的化合价为+5价.
某有机物4.4g在氧气中充分燃烧,生成13.2g二氧化碳和7.2g水.由此可确定该物质是由元素组成的,如果该物质的相对分子质量是44,该物质的化学式为.
化学与生活密切相关,身边处处有化学.
(1)用洗涤剂清洗油污,是利用洗涤剂的作用.
(2)在厨房中能用来除去水垢的物质是.
(3)生石灰常用作食品干燥剂,原因是(用化学方程式表示).
如图是某化学反应前后的微观过程示意图,其中" "、"
"、" "表示两种不同的原子.请根据图示回答:
"表示两种不同的原子.请根据图示回答: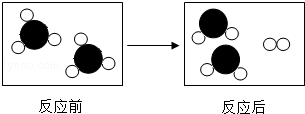
(1)该反应的基本类型是.
(2)反应前的物质(填"可能"或"不可能")是氧化物.
(3)反应前后 、
、 、
、 三种离子的个数比是.
三种离子的个数比是.
(4)从图中还可获得的一条消息是.