(9分)以下是教材中关于水的一些实验,根据所学水的知识回答下列问题:
 |
 |
 |
| A.水的沸腾 |
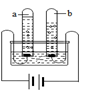
B.水的电解 |
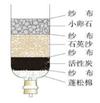
C.水的净化 |
(1)对于实验A水的沸腾,下列说法正确的是____________(填字母序号)
A.水分子之间间隔不变
B.水分子的运动速率加快
C.水分子保持不变
D.保持水化学性质的粒子是氢原子和氧原子
(2)实验B水的电解中试管b得到的气体是_____(填名称)。做该实验时,要在水中加入少量的氢氧化钠,目的是________________,若配制100g溶质质量分数为10%的氢氧化钠溶液进行水的电解实验,则需氢氧化钠的质量为:__ __ _g,量取水(水的密度为1g/cm3)应选择规格是 mL的量筒(选填“10”、“100”或“250”),电解一段时间后,溶液中溶质的质量分数会__ __ _10%(填“<”、“=”或“>”)。
(3)实验C中净化水时,活性炭的作用是______________。
(4)水是一种重要的化工原料。氯碱工业通过电解饱和氯化钠溶液的方法制取烧碱(NaOH),其中发生的主要反应是氯化钠和水在通电的条件下生成氢氧化钠、氢气、氯气,该反应的化学方程式为______ _______。
化学就在我们身边,它能改善我们的生活。请从“A.聚乙烯、 B. 氢氧化钙、 C食醋、D. 生石灰、E.碳酸钠、F. 甲烷”中选择适当的物质填空。
(1)厨房调味品中pH小于7的是(2)能用作食品干燥剂的是
(3)可以制成食品包装袋的是 (4)用于配制波尔多液的碱
(5)侯氏联合制碱法中的“碱”是(6)最简单的有机化合物
用数字和化学符号填空:
(1) 5个二氧化硫分子_________;(2) 1个铜原子________;(3) 2个碳酸根离子________;
|
(4) 氢氧化铁中铁元素的化合价为+3价___________;(5)氖气___________。
以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
Ⅰ.由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制。下图是粗盐精制的流程: 回答下列问题:
回答下列问题:
(1)操作②的名称是。
(2)在悬浊液中加NaOH溶液、Na2CO3溶液、BaCl2溶液三种试剂的顺序合理的为。
| A.先加入NaOH,后加入Na2CO3,再加入BaCl2溶液 |
| B.先加入NaOH,后加入BaCl2溶液,再加入Na2CO3 |
| C.先加入BaCl2溶液,后加入NaOH,再加入Na2CO3 |
| D.先加入BaCl2溶液,后加入Na2CO3,再加入NaOH |
有同学提出用溶液代替BaCl2溶液可达到同样的目的。
Ⅱ.下图是电解食盐水制取氯气、氢氧化钠等产品的流程: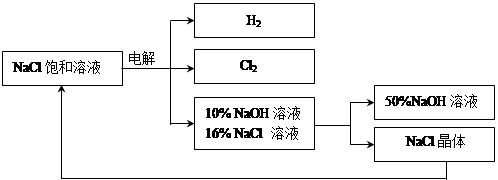
(3)在电解过程中,发生的反应为2NaCl + 2H2O Cl2 ↑+ H2 ↑ + 2NaOH,电解后溶液的pH。(填“升高”、“不变”、“降低”)
Cl2 ↑+ H2 ↑ + 2NaOH,电解后溶液的pH。(填“升高”、“不变”、“降低”)
(4) 电解食盐水时,需防止Cl2和NaOH反应,因Cl2和NaOH溶液充分接触会生成NaClO、氯化钠、水,请写出Cl2和NaOH溶液反应的化学方程式。
(5)该流程中可以循环利用的物质是。
(6)若取100g的溶质质量分数为25%的氯化钠溶液进行电解,一段时间后停止通电,生成氯气的质量7.1g。请计算:生成氢气的质量为多少克?反应后溶液中NaOH的质量分数是多少?(写出计算过程,计算结果精确到0.1%)
(7)若使(6)中电解后的溶液恢复到原来状态,则需向溶液中加入适量的。
4分)已知A、B、C、D、E、F为六种常见化合物,它们的相互反应及转化关系如图,B为参与植物光合作用的气体,E通常为无色液体,请回答:
(1)B的化学式为;(2)D的俗称是;
(3)D → F的反应属于基本类型为:。
(4)B与C反应生成E和F的化学方程式:。
有一种牙膏侧面的标签如图:
(1)测得牙膏与水的混合物的pH为8, 则其呈性(填“酸”、“中”或“碱”)。
(2)该支牙膏含氟元素的质量为 g。
(3)检验该牙膏中是否含有碳酸根离子的实验方法是。