污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物。某小组同学拟探究H2C2O4浓度对反应速率的影响。
实验仪器
I.实验原理
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
II.实验设计
(1)【方案一】测量气体产物:在相同温度下,利用下图装置,测定不同浓度H2C2O4溶液与KMnO4反应产生相同体积CO2所需的时间(忽略CO2溶解性的影响)。下图方框中应选择 (填编号)仪器组装量气装置,限选以下仪器:
①广口瓶、②双孔塞、③水槽、④橡胶管、⑤导管、⑥量筒、⑦秒表。
(2)【方案二】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间。拟定实验数据:
| 实验序号 |
温度/℃ |
各物质的体积 / mL |
反应时间 |
|||
| H2O |
3 mol/L稀硫酸 |
0.1mol/L KMnO4溶液 |
0.6 mol/LH2C2O4溶液 |
|||
| 1 |
25 |
3.0 |
2.0 |
4.0 |
6.0 |
t1 |
| 2 |
25 |
① |
2.0 |
4.0 |
4.0 |
t2 |
| 3 |
② |
7.0 |
2.0 |
4.0 |
2.0 |
t3 |
表中①、②处的数据分别是 、 。
III.讨论与交流
(3)小组同学在处理一系列的实验数据时,发现速率(v)-时间(t)曲线如下图所示。他们认为:0~t时间内,速率变快的可能原因是 。
(4)实验室常用KMnO4标准溶液滴定某浓度草酸。KMnO4溶液置于 (填仪器名称)中,判断到达滴定终点的现象是 。若滴开始时,滴定管中有气泡,滴定结束时气泡消失,则测定结果 (填“偏高”、“偏低”、“无影响”)。
海洋植物如海带.海藻中含有丰富的碘元素,其主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:(已知: 2I- + Cl2=2Cl-+ I2)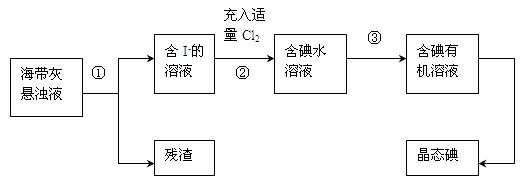
(1)指出提取碘的过程中有关的实验操作名称:①,③;
(2)过程②中充入适量Cl2的目的是;
(3)操作③中所用的有机试剂可以是(只填一种),
(4)操作过程③可以分解为如下几步:
| A.把盛有溶液的分液漏斗放在铁架台的铁圈中; |
| B.把50ml碘水和15ml有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞; |
| C.检验分液漏斗活塞和上口的玻璃塞是否漏液; |
| D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正; |
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
(a)过程③正确操作步骤的顺序是:(填编号字母);
(b)上述G步操作的目的是:;
标准状况下,1体积水中能溶解500体积的HCl气体。若向水中通入标准状况下的44.8LHCl气体配成1L溶液,假设气体完全溶解,得溶液中含HCl的物质的量浓度为;若得溶液密度为1.1g/cm3,则溶液中含HCl质量分数为;从该溶液中取出10mL浓盐酸溶解于水配制成250mL溶液,配制后的稀溶液中含HCl物质的量浓度为。在用浓盐酸配制上述稀盐酸时,所用仪器中,使用前必须检查是否漏液的仪器有;配制过程中,造成浓度偏低的操作可能有(选填下列操作的序号)。
| A.容量瓶蒸馏水洗后未加干燥 |
| B.量筒用蒸馏水洗后未干燥 |
| C.将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯,即向容量中加水到刻度 |
| D.用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚巧达刻度线 |
E、定容时,俯视液面加水至刻度线
工业上电解饱和食盐水能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)如图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是________;NaOH溶液的出口为________(填字母);精制饱和食盐水的进口为________(填字母);干燥塔中应使用的液体是________。
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为______________________。
②SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3SiCl4(g)+2H2(g)+Si(g) 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为________kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气________m3(标准状况)。
物质A~E中均含某种元素,都是中学化学中常见的物质,它们可发生如图所表示的反应(除A~E外的其它物质已略去):
(1)写出相应物质的类别:
| B |
C |
D |
|
| 类别 |
(2)在以上反应中(用序号填空):
属于氧化还原反应的是;属于复分解反应的是。
(3)写出反应③和⑦的离子方程式::。
某学生欲用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 。直到因加入一滴盐酸,溶液的颜色由色变为 ,且半分钟不褪色,即停止滴定。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是(填序号)。
| A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸 |
| B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
E. 滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若滴定开始和结束时,酸式滴定管中的液面如下图所示:则起始读数为ml,终点读数为ml。
(4)如已知用c(HCl)=1×10-2 mol/L的盐酸测定100mL的氢氧化钠溶液、测得c(NaOH)
mol/L