短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍或者C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和。下列说法正确的是
A.元素A所形成的氧化物只有一种
B.元素B的最高价氧化物对应的水化物为强酸
C.元素C、D、E的最高价氧化物对应的水化物两两之间可发生反应
D.氢化物的稳定性:A>B
在下列各说法中,正确的是
| A.ΔH>0表示放热反应,ΔH<0表示吸热反应 |
| B.热化学方程式中的化学计量数只表示物质的量,可以是分数 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
| D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
下列说法不正确的是
| A.化学反应除了生成新物质外,还伴随着能量的变化 |
| B.对于ΔH>0的反应,反应物的能量小于生成物的能量 |
| C.放热反应都不需要加热就能发生 |
| D.吸热反应在一定条件(如常温、加热等)下也能发生 |
已知:2CO(g)+O2(g)=2CO2(g) ΔH=" -566" kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ 1/2O2(g) ΔH=" -226" kJ/mol
根据以上热化学方程式判断,下列说法正确的是
| A.CO的燃烧热为566 kJ/mol |
B.图可表示由CO生成CO2的反应过程和能量关系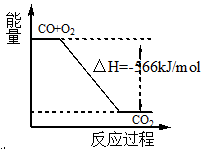 |
| C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)ΔH>-452 kJ/mol |
| D.CO2(g)与Na2O2(s)反应放出452kJ热量时,电子转移的物质的量为为2 mol |
反应C (s) + H2O (g)  CO (g) + H2 (g),在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO (g) + H2 (g),在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
| A.增加C的量 |
| B.将容器的体积缩小一半 |
| C.保持体积不变,充入N2使体系压强增大 |
| D.保持压强不变,充入N2使容器体积变大 |
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:

下列说法不正确的是
| A.该过程中CeO2没有消耗 |
| B.该过程实现了太阳能向化学能的转化 |
| C.右图中△H1=△H2+△H3 |
| D.H2(g)+ 1/2 O2(g) = H2O(g)的反应热大于△H3 |