常温下,下列溶液中各组离子一定能大量共存的是
| A.使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、CO32- |
| B.由水电离产生的c(H+)=10-12mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl- |
| C.c(H+)/c(OH-)= 1×1014的溶液: Ca2+、Na+、ClO-、NO3- |
D.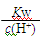 =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3- =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3- |
解释下列物质性质的变化规律与物质结构间的因果关系时,与氢键有关的变化规律是()
| A.HF、HCl、HBr、HI的热稳定性依次减弱 |
| B.熔点:Li> Na> K> Rb |
| C.NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D.H2S的熔沸点小于H2O的熔沸点 |
X、Y、Z、W为四种短周期元素,有关这四种元素的说法中一定正确的是( )
| 元素 |
X |
Y |
Z |
W |
| 原子半径(nm) |
0.077 |
0.075 |
0.102 |
0.099 |
| 最高正价或最低负价 |
+4 |
+5 |
-2 |
-1 |
A.1molW的单质参加氧化还原反应时转移的电子数为2mol
B. X与Z形成XZ2时各原子均满足8电子稳定结构
C.0.3molCu分别与足量HYO3和H2ZO4的稀溶液反应均产生0.2mol气体
D.Y的氢化物与W的氢化物反应的产物只含有共价键
现有四种元素的基态原子的核外电子排布式如下:
①1s22s22p63s23p4 ②1s22s22p63s23p3③1s22s22p3④1s22s22p5
则下列有关比较中正确的是 ( )
| A.第一电离能:④>③>②>① | B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:④>③=②>① |
向下例配合物的水溶液中加入AgNO3溶液,不能生成AgCl沉淀的是()
| A.[Co(NH3)5Cl]Cl2 | B.[Co(NH3)6]Cl3 |
| C.[Co(NH3)3Cl3] | D.[Co(NH3)4Cl2]Cl |
下列晶体中既含有离子键又含有极性共价键和配位键的是()
| A.NaCl | B.H2SO4 | C.NH4Cl | D.Na2O2 |