某同学在电视寻宝节目中,看到一些铜制文物上有绿色的锈迹,并对绿色锈迹产生了探究兴趣。
【查阅资料】①绿色锈迹是碱式碳酸铜[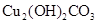 ],受热易分解。
],受热易分解。
②无水硫酸铜为白色粉末,遇水变蓝。
③碱石灰是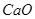 和
和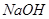 的固体混合物,
的固体混合物,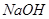 与
与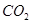 反应生成碳酸钠固体和水。
反应生成碳酸钠固体和水。
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁
上有无色液滴生成。为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体的成分。
【猜想与假设】该黑色固体可能是①碳粉;② ;③碳和氧化铜的混合物。
【设计方案】请帮助该同学完成下述实验报告。
| 实验操作与现象 |
实验结论 |
| |
猜想②正确 |
探究二:碱式碳酸铜受热分解还会生成CO2和H2O。
【进行实验】选择如下图所示装置进行验证。
步骤一:连接A和B,打开活塞,通入一段时间的空气。
步骤二,关闭活塞,依次连接装置A→B→ → (填“C”、“D”)。
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
【解释与结论】
①当观察到 ,说明碱式碳酸铜受热分解生成了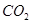 和
和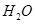 ,写出C中反应的化学方程式 。
,写出C中反应的化学方程式 。
②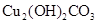 受热分解的化学方程式 。
受热分解的化学方程式 。
【反思与评价】
上述装置中A的作用是 。
某化工厂的废液中,可能含有H2SO4、K2CO3、Na2SO4、KCl、FeCl3、HNO3六种物质中的两种。进行有关试验,所观察到的现象记录如下表。试根据各步实验及其现象进行分步推断,再推断所取的废液的可能组合。
| 步骤 |
实验操作 |
实验现象 |
推断(或结论) |
| (1) |
取废液放入试管观察 |
废液中肯定不含FeCl3 |
|
| (2) |
用广泛pH试纸测定废液的pH |
测定结果:pH=3 |
|
| (3) |
向废液中滴入足量溶液 |
有白色沉淀出现 |
有硫酸或硫酸钠 |
| (4) |
向上述过滤所得的滤液中滴加AgNO3溶液 |
无明显反应现象 |
|
| 废液成分的可能组合(写出溶质的化学式) |
①_____________________ ②H2SO4、HNO3 ③_____________________ |
(9分))同学们在学习碱的化学性质时,进行了如图所示的实验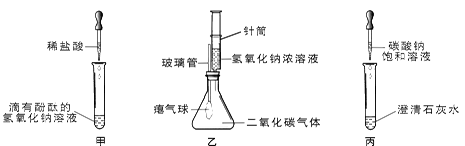
(1)写出甲实验中盐酸和氢氧化钠的反应。
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是。
(3)丙实验中观察到试管内有白色沉淀产生。
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色。
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、水和(写物质名称)。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有
如下猜想。
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
【实验设计】小方想用氯化钙溶液来验证小云、小红、小林的猜想。查阅资料获悉氯化钙、氯化钠溶液呈中性,并设计如下实验。请你将小方的实验设计补充完整。
| 实验内容 |
现象 |
结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置。 |
①有白色沉淀,溶液呈红色 ② ③ |
的猜想正确 小云的猜想正确 的猜想正确 |
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑
。
氢氧化钠溶液与稀硫酸发生中和反应时观察不到明显现象,为了确定其反应是否反生,某班同学设计了不同的实验方案进行探究:
(1) 方案一:向装有一定量氢氧化钠溶液的烧杯中滴几滴酚酞试液,不断滴入稀硫酸,并用玻璃棒搅拌。如果实验现象是________________就可以证明氢氧化钠溶液与稀硫酸发生了化学反应;其反应的化学方程式为_______________________________;
(2)方案二:向装有一定量稀硫酸的试管中滴加氢氧化钠溶液,振荡后再向其中滴加碳酸钠溶液,如果有气泡产生,则说明氢氧化钠溶液与稀硫酸没有发生化学反应。你认为方案二的结论正确吗?___________(填“正确”或“不正确”),理由是: _____________________
(3)下列实验方案中,能证明氢氧化钠溶液与稀硫酸发生了反应的是_____________(填序号)。
A.用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,pH逐渐减少,最终小于7
B.用温度计测试氢氧化钠溶液滴加稀硫酸前后的温度,温度明显上升
C.向一定量的氢氧化钠溶液中滴加稀硫酸后再滴加硫酸铜溶液,有蓝色沉淀生成
请从下列物质中选择适当的试剂,设计不同的方法对锌、铁、铜三种金属的活动性顺序进行探究:
| A.锌片 | B.铁钉 | C.铜片 | D.硫酸铜 E.稀硫酸 F.硫酸锌 G.硫酸亚铁。 |
(1)方法一所选用的三种试剂是CuSO4、ZnSO4和____(填化学式,下同)。
(2)方法二所选用的是四种试剂是Fe、Cu、Zn和____。
以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20
;"浓度"指溶质的质量分数)
| 实验序号 |
过氧化氢溶液浓度/% |
过氧化氢溶液质量/ | 温度/ | 二氧化锰用量/ | 氧气体积/ | 反应所需时间/ |
| ① |
5 |
12 |
20 |
0.2 |
125 |
11 |
| ② |
30 |
12 |
20 |
0.2 |
125 |
2 |
| ③ |
30 |
12 |
40 |
/ |
125 |
148 |
| ④ |
30 |
12 |
90 |
/ |
125 |
82 |
(2)通过对比实验和可知,化学反应快慢与温度的关系是.
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是.
(4)某实验室需配置450克5%的过氧化氢溶液,其操作为:往一定量30%的过氧化氢溶液中加入克水,然后用(填仪器名称)搅拌均匀.