下列试剂可用带玻璃塞的玻璃试剂瓶保存的是
| A.氢氟酸 | B.硫酸 | C.碳酸钠溶液 | D.氢氧化钠溶液 |
现代生产、生活和国防中大量使用电池。下列有关电池的说法正确的是
| A.碱性锌锰电池性能好于普通电池的原因是能反复使用 |
| B.碱性锌锰电池的正极是MnO2,当电池中有6.5g Zn反应时,将产生0.2molMnOOH |
| C.铅蓄电池放电时,负极的质量减少 |
| D.使用碱性电解质的氢氧燃料电池,负极的电极反应是H2 - 2e- = 2H+ |
以下是碘与氢气反应的热化学方程式,有关判断正确的是
(ⅰ) I2(g)+H2(g) 2HI(g) ΔH=-9.48 kJ/mol
2HI(g) ΔH=-9.48 kJ/mol
(ⅱ) I2(s)+H2(g) 2HI(g) ΔH=+26.48 kJ/mol
2HI(g) ΔH=+26.48 kJ/mol
| A.1 mol I2(g)中通入1 mol H2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.分解1 mol HI (g)生成H2(g)和固态碘的反应吸热13.24kJ |
| D.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低 |
下列叙述正确的是
| A.把纯水加热,水的电离程度增大,但水仍然是中性的,pH=7 |
| B.在醋酸溶液中加入少量的CH3COONa(s),测得pH变大,主要原因是CH3COONa水解呈碱性,中和醋酸电离的H+ |
| C.pH=3的醋酸溶液,稀释至10倍后pH<4 |
| D.相同浓度的CH3COONa溶液与Na2CO3溶液相比,Na2CO3溶液的pH小 |
铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是
①实验过程中取出盐桥,原电池仍继续工作
②将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
③负极反应为:Ag+ + e- = Ag
④盐桥内的K+移向AgNO3溶液
| A.②④ | B.①② | C.②③ | D.③④ |
下列叙述中正确的是
| A.稀醋酸与稀氢氧化钠溶液发生中和反应的热化学方程式为 CH3COOH (aq) + NaOH (aq) = CH3COONa(aq) + H2O(l) ΔH = 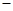 57.3kJ/mol 57.3kJ/mol |
| B.在101kPa时1mol物质燃烧时的反应热叫做该物质的燃烧热 |
| C.未来氢气作为新能源的其中一个优点是充分燃烧的产物不污染环境 |
| D.升高温度或加入催化剂,可以改变化学反应的反应热 |