在CuO和Fe粉的混合物中,加入一定量的稀硫酸,并微热,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,发现铁钉并无任何变化。根据上述现象,确定下面结论正确的是
| A.不溶物一定是Cu | B.不溶物一定含铜,但不一定含铁 |
| C.不溶物一定是Fe | D.滤液中一定含有Fe2+,但不一定含有Cu2+ |
某非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素
| A.在自然界中只以化合态的形式存在 | B.单质常用作半导体材料和光导纤维 |
| C.最高价氧化物能与水反应生成酸 | D.常温下与氯气反应 |
工业炼铁,用到的原料有:铁矿石、焦炭、空气、石灰石,下列对原料在冶炼过程中的
作用叙述不正确的是
| A.焦炭是铁矿石炼铁时的还原剂 | B.空气在与焦炭的反应中,为炼铁提供能量 |
| C.石灰石是助矿石中杂质形成炉渣 | D.固体原料需粉碎,增大与气体的接触面 |
在K37ClO3 + 6HCl == KCl + 3Cl2↑+ 3H2O反应中
| A.氧化产物与还原产物物质的量比是3:1 |
| B.被氧化的HCl占参加反应HCl总量的5/6 |
| C.K37ClO3只有一部分发生还原反应 |
| D.反应完成后37Cl存在于KCl |
在下列反应中,HNO3既表现出氧化性,又表现出酸性的是
A.H2S+2HNO3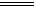 S↓+2NO2↑+2H2O S↓+2NO2↑+2H2O |
B.CuO+2HNO3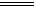 Cu(NO3)2+H2O Cu(NO3)2+H2O |
C.4HNO3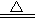 4NO2↑+O2↑+2H2O 4NO2↑+O2↑+2H2O |
D.3Cu+8HNO3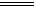 3Cu(NO3)2+2NO↑+4H2O 3Cu(NO3)2+2NO↑+4H2O |
.用NA表示阿伏加德罗常数,下列叙述正确的是
| A.1 mol Cl2参加反应转移电子数一定为2 NA |
| B.常温常压下,含有6.02×1024个电子的重水(D2O)的质量约为18 g |
| C.常温常压下,NA个CO2分子占有的体积大于22.4L |
| D.0.5 mol·L-1 Na2SO4溶液中所含Na+的数目为NA |