甲、乙、丙是中学化学常见物质,一定条件下能发生转化:甲+强酸→乙十丙十H2O ,其中乙为盐,丙为气体。下列说法正确的是
| A.甲一定是金属单质 | B.甲与乙一定含有同种元素 |
| C.丙一定是氧化物 | D.该反应一定是氧化还原反应 |
下列热化学方程式中△H的绝对值表示可燃物燃烧热的是
A.CO(g)+ 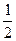 O2(g) ===CO2(g O2(g) ===CO2(g )△H=-283.0 kJ·mol-1 )△H=-283.0 kJ·mol-1 |
| B.CH4(g)+ 2O2(g) ===CO2(g)+2H2O(g)△H=-802.3 kJ·mol-1 |
| C.2H2(g)+ O2(g) ===2H2O(l)△H=-571.6kJ·mol-1 |
D.C(s)+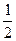 O2(g) ===CO(g)△H=-110.5kJ·mol-1 O2(g) ===CO(g)△H=-110.5kJ·mol-1 |
下列说法中错误的是
| A.许多化学反应中的能量变化表现为热量的放出和吸收 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.选择燃料只需要考虑燃料热值的大小 |
| D.若反应物总能量大于生成物总能量则反应为放热反应 |
能正确表示下列反应的离子方程式是
| A.苯酚钠溶液与少量二氧化碳反应:C6H5O-+CO2+H2O=C6H5OH+CO32- |
| B.碳酸氢钙与过量的NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| C.醋酸钠的水解反应:CH3COO-+H2O=CH3COOH+OH- |
| D.稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O |
以下实验:①为检验RI(碘代烷)中的碘元素,将RI与NaOH水溶液混合共热后再加入AgNO3溶液;②实验室里用无水乙醇和浓硫酸共热至140℃制乙烯;③用锌与稀硝酸反应制取氢气,并用排水法收集氢气;④在试管中加入2mL 10%的CuSO4溶液,滴入2%的NaOH溶液4~6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾;⑤为检验淀粉已水解,将淀粉与少量稀硫酸加热一段时间后再加入银氨溶液,水浴加热;⑥将饱和氯化铁溶液煮沸,制备氢氧化铁胶体。可能失败的实验是
| A.①②③④⑤⑥ | B.只有①④⑤ | C.只有③④⑤ | D.只有②③⑤⑥ |
下列说法中,正确的是
| A.原子晶体的熔点一定高于离子晶体的熔点 |
| B.第三周期主族非金属元素的氧化物对应的水化物的酸性,从左到右逐渐增强 |
| C.-OH与OH-是不同的微粒,电子式和稳定性各不相同 |
| D.蛋白质、油脂、淀粉等都是人类的重要营养物质,它们都是天然高分子化合物 |