用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH同时得到某种副产物,其原理如图所示(电极材料为石墨)。下列说法不正确的是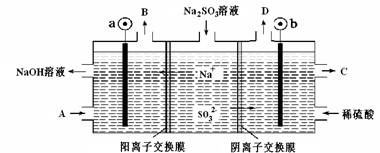
| A.b电极上的主反应是 SO32--2e-+H2O===SO42-+2H+ |
| B.若D是混合气体,则可能含有SO2、O2等成分 |
| C.a 电极发生还原反应,当有1mol Na+通过阳离子交换膜时,a极生成11.2L气体 |
| D.A溶液是稀NaOH溶液,作用是增强溶液的导电性;C是较浓的硫酸溶液 |
下列事实不能用电化学原理解释的是()
| A.常温条件下,在空气中铝不容易被腐蚀 |
| B.镀锌铁片比镀锡铁片更耐腐蚀 |
| C.用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 |
| D.远洋海轮的尾部装上一定数量的锌板 |
下列叙述中正确的是()
①锌跟稀硫酸制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破坏后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③钢铁表面常易锈蚀生成 Fe2O3 · H2O
| A.都正确 | B.①③ | C.① | D.②③ |
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)  2C(g)
2C(g)
若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1
②用物质B表示的的反应的平均速率为0.6 mol·L-1·s-1
③2 s时物质A的转化率为70%④2 s时物质B的浓度为0.7 mol·L-1,其中正确的是
| A.①③ | B.①④ | C.②③ | D.③④ |
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO )=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.原混合溶液中c(K+)为0.2 mol·L-1 |
| B.上述电解过程中共转移0.2 mol电子 |
| C.电解得到的Cu的物质的量为0.05 mol |
| D.电解后溶液中c(H+)为0.2 mol·L-1 |
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1 mol时,下列说法不正确的是( )。
| A.溶液的质量变化:甲减小乙增大 |
| B.溶液pH变化:甲减小乙增大 |
| C.相同条件下产生气体的体积:V甲=V乙 |
| D.电极反应式:甲中阴极为Cu2++2e-===Cu,乙中负极为Mg-2e-===Mg2+ |