下列说法正确的是
| A.反应热就是反应中放出的能量 |
| B.在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 |
| C.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
| D.由C(石墨)===C(金刚石) ΔH=+1.9 kJ·mol-1可知,金刚石比石墨稳定 |
已知298K时反应2SO2( g )+ O2( g )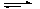 2SO3( g );△H =" -197" kJ · mol-1,在相同温度下向一密闭容器中加入2 mol SO2和1 molO2,达化学平衡时放出热量为a1 kJ ;向另一容积相同的密闭容器中通入 1 mol SO2和0.5 molO2,达化学平衡时放出热量为a2 kJ ,则下列关系式中正确的是
2SO3( g );△H =" -197" kJ · mol-1,在相同温度下向一密闭容器中加入2 mol SO2和1 molO2,达化学平衡时放出热量为a1 kJ ;向另一容积相同的密闭容器中通入 1 mol SO2和0.5 molO2,达化学平衡时放出热量为a2 kJ ,则下列关系式中正确的是
| A.a2<a1< 197 | B.2a2>a1 >197 |
| C.2a2 = a1 >197 | D.2a2 = a1 = 197 |
对达到平衡状态的可逆反应A+B  C+D,在t1时增大压强,正、逆反应速率变化图象如图所示,下列有关A、B、C、D的状态叙述正确的是
C+D,在t1时增大压强,正、逆反应速率变化图象如图所示,下列有关A、B、C、D的状态叙述正确的是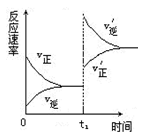
A.A、B、C为气体,D不是气体
B.A、B为气体,C、D有一种为气体
C.C、D为气体,A、B有一种为气体
D.A、B、C、D都不是气体
可逆反应aX+2Y(g)⇌2Z(g)在一定条件下的达到平衡后,t1和t2时各改变某一种外界条件,化学反应速率(v)﹣时间(t)图象如图。则下列说法中正确的是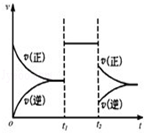
| A.若X是固体,则t1时一定是增大了容器的压强 |
| B.若X是气体,则t2时不可能是减小容器压强 |
| C.若X是固体,则t1时可能是增大了X的质量 |
| D.若t2时采用了降温措施,则该反应的正反应方向△H>0 |
在2L的密闭容器中,发生3A(g)+B(g) 2C(g)的反应,若最初加入A和B都是4mol,测得10s内A的平均速率v(A)=0.12mol/(L.s),则反应进行到10s时容器中B的物质的量是
2C(g)的反应,若最初加入A和B都是4mol,测得10s内A的平均速率v(A)=0.12mol/(L.s),则反应进行到10s时容器中B的物质的量是
A.1.6mol B.2.8mol C.3.2molD.3.6mol
科学家发现,不管化学反应是一步完成还是分几步完成,该反应的热效应是相同的。已知在25℃,105 Pa时,1 mol石墨和1 mol一氧化碳完全燃烧生成二氧化碳时的放热分别 是ΔH=-393.5 kJ/mol和ΔH=-283 kJ/mol,下列说法或方程式正确的是
| A.在相同条件下,C(石墨,s)+CO2(g)===2CO(g)ΔH=+172.5 kJ/mol |
| B.1 mol石墨不完全燃烧,生成CO2和CO混合气体时,放热504.0 kJ |
| C.2C(石墨,s)+O2(g)===2CO(g)ΔH=-110.5 kJ/mol |
| D.已知金刚石不如石墨稳定,则石墨转变为金刚石需要放热 |