下列说法中正确的是
| A.已知H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应、稀醋酸与稀NaOH溶液反应所测得的中和热都为ΔH=-57.3kJ/mol |
| B.由C(石墨,s)= C(金刚石,s)ΔH=+1.9kJ/mol,可知金刚石比石墨稳定 |
| C.在用标准盐酸滴定未知浓度氢氧化钠溶液的实验中,若用待测液润洗锥形瓶,则测定结果偏低(其他操作正确) |
D.向存在着FeCl3 (黄色)+3KSCN  Fe(SCN) 3(血红色) +3KCl平衡体系的溶液中,加少量KCl固体,溶液血红色不发生变化 Fe(SCN) 3(血红色) +3KCl平衡体系的溶液中,加少量KCl固体,溶液血红色不发生变化 |
将足量CO2通入下列各溶液中,所含离子还能大量共存的是()
A. |
B. |
C. |
D. |
将足量CO2通入KOH和Ca(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(V)的关系正确的是()
下列有关说法正确的是()
| A.CO2、CH4、N2等均是造成温室效应的气体 |
| B. 14C可用于文物鉴定,14C与12C互为同素异形体 |
| C.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
D.精炼粗铝时要清除坩埚表面的石英砂,铝与石英砂反应的方程式为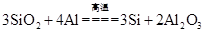 |
可以用来检验碳酸氢钠粉末中是否混有碳酸钠的实验方法是()
| A.加热,看有无气体放出 |
| B.滴加盐酸,看有无气体放出 |
| C.溶于水后,滴加稀的氯化钡溶液看有无白色沉淀生成 |
| D.溶于水后,滴加澄清石灰水看有无白色沉淀生成 |
下列关于硅单质及其化合物的说法正确的是()
①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料
| A.①② | B.①④ | C.②③ | D.③④ |