碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Al(OH)3 |
| 开始沉淀 |
2.3 |
7.5 |
3.4 |
| 完全沉淀 |
3.2 |
9. 7 |
4.4 |
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在 范围内。
(2)反应Ⅱ中加入NaNO2的目的是氧化亚铁离子,写出该反应的离子方程式为 。
(3)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为 。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为 。
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
(5)为测定含Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00mL溶液于带塞锥形瓶中,加入足量H2O2,调节pH<2,加热除去过量H2O2;加入过量KI充分反应后,再用 0.1000 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
已知:
则溶液中铁元素的总含量为 g·L-1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将
会 (填“偏高” “偏低” “不变”)
亚硫酸盐是一种常见食品添加剂。为检验某食品中亚硫酸盐含量(通常
样品中含
的质量计),某研究小组设计了如下两种实验流程:
(1)气体
的主要成分是,为防止煮沸时发生暴沸,必须先向烧瓶中加入;通入N2的目的是。
(2)写出甲方案第①步反应的离子方程式:。
(3)甲方案第②步滴定前,滴定管需用
标准溶液润洗,其操作方法是。
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果(填"偏高"、"偏低"或"无影响")
(5)若取样品
,按乙方案测得消耗0.01000
溶液
,则1
样品中含
的质量是g(用含
的代数式表示)。
实验室常用
与浓盐酸反应制备
(发生装置如图所示)。
(1)制备实验开始时,先检查装置气密性,接下来的操作依次是(填序号)
A.往烧瓶中加人
粉末
B.加热
C.往烧瓶中加人浓盐酸
(2)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
甲方案:与足量
溶液反应,称量生成的
质量。
乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量
(过量)反应,称量剩余的
质量。
丁方案:与足量
反应,测量生成的
体积。
继而进行下列判断和实验:
① 判定甲方案不可行,理由是。
② 进行乙方案实验:准确量取残余清液稀释一定倍数后作为试样。
a.量取试样20.00
,用0.1000
标准溶液滴定,消耗22.00
,该次滴定测得试样中盐酸浓度为
b.平行滴定后获得实验结果。
③ 判断丙方案的实验结果(填"偏大"、"偏小"或"准确")。
) = 2.8×10-9、
= 2.3×10-11
④ 进行丁方案实验:装置如图所示(夹持器具已略去)。
(i) 使Y形管中的残余清液与锌粒反应的正确操作是将转移到中。
(ii)反应完毕,每间隔1 分钟读取气体体积,气体体积逐次减小,直至不变。气体体积逐次减小的原因是(排除仪器和实验操作的影响因素)。
甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计如下实验流程:
实验中,先用制的的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完毕后,黑色的氧化铜转化为红色的铜。
下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。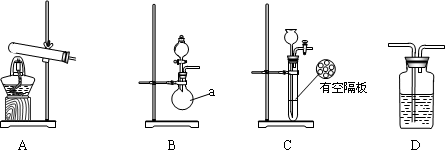
甲小组测得,反应前氧化铜的质量
、氧化铜反应后剩余固体的质量
、生成氮气在标准状况下的体积
。
乙小组测得,洗气前装置D的质量
、洗气后装置D的质量
、生成氨气在标准状况下的体积
。
请回答下列问题:
(1)写出仪器a的名称。
(2)检查A装置气密性的操作是。
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写在下表的空格中。
| 实验装置 |
实验药品 |
制备原理 |
|
| 甲小组 |
A |
氢氧化钙、硫酸、硫酸铵 |
反应的化学方程式为。 |
| 乙小组 |
浓氨水、氢氧化钠 |
用化学平衡原理分析氢氧化钠的作用:。 |
(4)甲小组用所测得数据计算出氨分子中氮、氢的原子个数之比为。
(5)乙小组用所测得数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是
。为此,乙小组在原有实验的基础上增加了一个装有某药品的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氨气的体积,得出了合理的实验结果。该药品的名称是。
某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质,首先做了银镜反应.
(1)在甲酸进行银镜反应前,必须在其中加入一定量的,因为;
(2)写出甲酸进行银镜反应的化学方程式:
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作________(写字母):
| A.用洁净的试管; |
| B.在浓度为2%的NH3·H2O中滴入稍过量的浓度为2%的硝酸银; |
| C.用前几天配制好的银氨溶液; |
| D.在银氨溶液里加入稍过量的甲酸; |
E、用小火对试管直接加热;
F、反应过程中,振荡试管使之充分反应.
然后,同学们对甲酸与甲醇进行了酯化反应的研究:
(4)乙装置中长导管A的作用是;
(5)写出甲酸和甲醇进行酯化反应的化学方程式
(6)选择甲装置还是乙装置好?________,原因是;
(7)实验过程中选用的药品及试剂有:浓H2SO4、甲醇、甲酸还有________、________两种必备用品.
(8)一同学用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,
请给予合理的解释。
请你与某小组的同学共同探究乙醇与乙酸的酯化反应实验: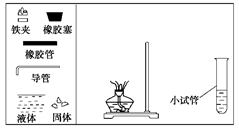
(1) 请你根据图示,补画实验室制取乙酸乙酯的装置图。
(2) 其中小试管中装入的物质是____________;其主要作用是、____________、__________________________。
(3) 分离小试管中制取的乙酸乙酯应使用的仪器叫做______________;分离完毕,应从该仪器________________ (填“下口放”或“上口倒”)出。
(4) 实验完毕,发现大试管中的反应液有些变黑,其原因是________________________。
(5) 该实验中,若用3mol乙醇和1mol乙酸在浓硫酸作用下加热,充分反应后,能否生成1mol乙酸乙酯? (填“能”或“不能”),原因是 (不考虑原料损耗)。
(6) 写出该反应的化学方程式: