(8分)小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
【作出猜想】
猜想一:Cr>Fe>Cu;猜想二:Fe>Cu>Cr;猜想三:你的猜想是 。
【查阅资料】
铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮,分别放入等量的同种稀硫酸。
【结论与解释】
(1)小聪得到的结论是猜想 正确。
(2)实验前用砂纸打磨金属片的目的是 。
【知识运用】
将铬片投入FeSO4溶液中,反应 (填“能”或“不能”)进行。若能进行,请你写出反应的化学方程式 。
生产、生活、科技、环保等都离不开化学.
Ⅰ.食品、药物安全一直是人们关注的话题.
(1)2012年4月17日经央视新闻频道曝光的用工业明胶制成的医用“毒胶囊”震惊全国.据悉,其中混有的重金属铬对人体有害.这里的铬是指________(填“元素”或“单质”).
(2)我市盛产的海产品鱼虾中富含基本营养素中的________(填“糖类”“油脂”或“蛋白质”).海产品容易腐烂变质,________(填“能”或“不能”)用甲醛溶液浸泡海产品防腐保鲜.
Ⅱ.材料的应用与发展,大大方便了人们的生活.请用下列三种材料的对应字母填空.
(A)有机合成材料
(B)金属材料
(C)天然有机高分子材料
(1)塑料制品属于________.
(2)棉花、羊毛属于________.
(3)可用于制造人造骨、航天飞机等的钛合金属于________.
Ⅲ.节能、减排、低碳、环保是当今世界的主旋律.
(1)开发________等新能源,不仅可以部分解决化石能源紧缺问题,还可以减少对环境的污染.
(2)煤燃烧时加入适当的物质,可以减少________气体(写化学式)和氮氧化物等有害气体的排放,有效减少酸雨的形成.
化学与健康——从化学的视角看食品添加剂.
近年来,食品添加剂成了国内外食品安全与健康饮食的焦点问题,如三聚氰胺、瘦肉精、染色馒头、毒豆芽……据《人民日报》报道,目前我国有近90%的食品中含有合法或违法的食品添加剂.那么,如何科学地看待食品添加剂?
我们知道,化学是认识物质、改造物质和应用物质的科学,从化学视角看食品添加剂,主要是从其元素组成与结构、物理化学性能及在人体内的变化等方面着眼.下表中给出了4种食品添加剂,试回答有关问题:
(1)请你在下表空白处填上物质的化学式.
| 物质组成与性能 |
被用于食品添加剂 |
|||
| 物质名称 |
物质组成(填化学式) |
主要化学性质及在体内变化 |
类别或作用 |
法律规定 |
| 碳酸氢钠 |
无毒、弱碱性、易与胃酸反应 |
蓬松剂 |
可用 |
|
| 硫酸铜 |
— |
增色 |
国家严禁使用 |
|
| 铁(还原性铁粉) |
比较活泼的金属,能与胃酸反应 |
抗氧化剂 |
依据国家标准,可用 |
|
| 甲醛 |
CH2O |
— |
防腐 |
国家严禁使用 |
(2)从应用物质的角度,人们常常根据物质的性质对物质进行分类,其原因在于________________________________.从性质上看,国家严格禁止甲醛和硫酸铜作为食品添加剂,是因为________________________________________________________________.在研究或认识物质的性质时,又常常根据物质的组成和结构对物质进行分类,其原因在于________________________________.
(3)还原性铁粉用于食品添加剂,除能够防止食品因氧化而变质外,还是一种营养强化剂,这是因为____________________________________________________________________
________________________________.
(4)碳酸氢钠是面食类食品经常使用的添加剂,如蒸馒头时人们常常加适量的碳酸氢钠.即使少量碳酸氢钠进入体内,也不会危害人体健康.请你从碳酸氢钠的性质、在胃液中的变化以及人体所必需的营养元素三个方面,解释为什么它不会对人体产生危害.________________________________.
(5)在改善食品的色香味、延长食品的保质期等方面,食品添加剂确实提高了现代食品的品质,但副作用也是显而易见的.我们需要食品添加剂吗?现在有两种观点:(A)可依法添加使用.(B)应禁止使用,因为绝大多数食品添加剂都是化学合成物质,对人体有害,而且违法滥用现象严重,影响人体健康.从化学的视角,你的观点是(填“A”或“B”)__________________________________________________.
维生素C又名抗坏血酸,易溶于水,易被氧化,能与碘反应.人体缺乏维生素C可引发多种疾病.某研究性学习小组对它研究如下:
(1)猜想:维生素C可能具有酸性.
(2)实验方案:提供的试剂有维生素C片、蒸馏水、紫色石蕊溶液、无色酚酞溶液、氢氧化钠溶液、pH试纸.(实验仪器自选)
根据以上用品,请你帮助他们设计出两种实验方案,并写出实验现象:
| 实验内容 |
实验内容 |
实验现象 |
| 方案I |
||
| 方案Ⅱ |
(3)结论:维生素C具有酸性.根据维生素C的性质,判断下列物质中能与维生素C反应的是()
(A)金属镁
(B)氯化钾
(C)氢氧化钠
(D)硫酸铜
(4)某同学联想到西红柿等蔬菜、水果中含有丰富的维生素C,则其放置时间的长短是否对维生素C的含量产生影响?他设计了如下的实验方案:
Ⅰ.把新鲜西红柿和放置一周的西红柿分别捣碎,用纱布将汁液挤入两个烧杯中.
Ⅱ.取两支盛有2mL蓝色的碘的淀粉溶液的试管,分别滴加上述两种汁液,边加边振荡,直到蓝色刚好消失,记录滴数如下:
| 汁液 |
新鲜西红柿的汁液 |
放置一周的西红柿的汁液 |
| 滴数 |
12 |
20 |
请回答下列问题:
①你认为维生素C含量较高的是________.
②你从中得到的启示是________________________.
葡萄糖是生命体所需能量的主要来源.
[提出问题]葡萄糖的完全燃烧产物是CO2和H2O,由此能否证明葡萄糖是只由碳元素和氢元素组成的有机物?
[实验设计]为了确定葡萄糖的元素组成,某小组设计了如下实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略).
(1)装置A中发生反应的化学方程式是________________________.
(2)装置B中浓硫酸的作用是________________________.
(3)装置C处氧化铜的作用是________________________.
[方案评价]
(1)用充有空气的储气球代替装置A,是否更有利于实验的进行?________(填“是”或“否”),原因是________________________________.
(2)装置C处葡萄糖燃烧的设计特点是________________________________________(至少写1条).
[数据处理]下表是同学们填写的实验报告,请你帮助完成.
| 实验事实 |
数据分析及结论 |
| 1.8g葡萄糖完全燃烧,得到2.64g CO2和1.08g H2O |
数据分析:________________ ________________________ ________________________ 结论:葡萄糖含有C、H、O三种元素 |
[讨论交流]为了尽量减少误差:
(1)该实验在进行过程中应注意的问题是________________________________________
____________________________________________________________________(写1条).
(2)从定量实验的角度看,该实验可进一步改进,请简要写出一个改进意见:________
________________________________________________________________________.
某同学家中有一袋化肥,可能混入了其他化肥,且化肥包装袋上的字迹模糊.该同学进行了如下探究,请你参与探究并填空:
[提出问题]该化肥中含有什么物质?
[收集信息]经询问得知,该化肥为铵态氮肥.
[提出猜想]该化肥所含的阴离子可能是Cl-、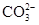 、
、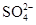 ;中的一种或几种.
;中的一种或几种.
[实验、记录与分析]
| 实验操作步骤 |
实验现象 |
实验分析 |
| (1)取少量该化肥样品和少量熟石灰放在研钵中混合研磨 |
________ |
含有铵根离子 |
| (2)另取少量该化肥样品于试管中,加入适量的水完全溶解,滴加足量的硝酸钡溶液,再滴加少量稀硝酸,过滤 |
产生白色沉淀,沉淀不溶解 |
没有________(填化学式)存在 |
| (3)取(2)中所得滤液少量于试管中,滴加________ |
________ |
有Cl-存在 |
[实验结论]若该化肥中只含有一种阳离子,则其中一定含有的物质是(写化学式)________________________________________________________________________.
[实验反思]若步骤(2)中用氯化钡溶液代替硝酸钡溶液是否可行?________(填“是”或“否”),请简要说明原因:________________________________________.